题目内容
下面关于氢化物的叙述正确的是( )
| A、一个D2O分子所含的中子数为8 |
B、NH3的结构式为: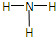 |
C、HCl的电子式为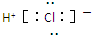 |
| D、热稳定性:HCl>HF |
考点:电子式、化学式或化学符号及名称的综合,元素周期律的作用
专题:化学用语专题
分析:A.每个D原子中含有一个中子、一个O原子含有8个中子;
B.氨气分子中N原子含有3个共价键和一个孤电子对;
C.HCl是共价化合物,H原子和Cl原子之间存在一个共用电子对;
D.非金属的非金属性越强,其氢化物越稳定.
B.氨气分子中N原子含有3个共价键和一个孤电子对;
C.HCl是共价化合物,H原子和Cl原子之间存在一个共用电子对;
D.非金属的非金属性越强,其氢化物越稳定.
解答:
解:A.每个D原子中含有一个中子、一个O原子含有8个中子,所以一个D2O分子所含的中子数为10,故A错误;
B.氨气分子中N原子含有3个共价键和一个孤电子对,其结构式为 ,故B正确;
,故B正确;
C.HCl是共价化合物,H原子和Cl原子之间存在一个共用电子对,其电子式为 ,故C错误;
,故C错误;
D.非金属的非金属性越强,其氢化物越稳定,非金属性F>Cl,所以热稳定性HF>HCl,故D错误;
故选B.
B.氨气分子中N原子含有3个共价键和一个孤电子对,其结构式为
 ,故B正确;
,故B正确;C.HCl是共价化合物,H原子和Cl原子之间存在一个共用电子对,其电子式为
 ,故C错误;
,故C错误;D.非金属的非金属性越强,其氢化物越稳定,非金属性F>Cl,所以热稳定性HF>HCl,故D错误;
故选B.
点评:本题考查了化学用语,明确原子构成、电子式书写规则、元素周期律即可解答,注意共价化合物和离子化合物电子式书写区别.

练习册系列答案
相关题目
“细节决定成败”对于下列实验细节处理正确的是( )
| A、实验室制氢气:为了加快反应速率,向稀H2SO4滴加少量CuSO4溶液 |
| B、钠与水的反应:取绿豆大小的金属钠放入烧杯,再滴入两滴酚酞试液,最后加入水 |
| C、配置0.10mol/L NaOH溶液:称取0.4g NaOH放入100mL容量瓶,加水至100mL |
| D、配置FeCl2溶液:称取一定量的FeCl2固体,加水溶解,在加入稀盐酸酸化 |
下列反应中离子方程式的书写正确的是( )
| A、向Na2CO3溶液中逐滴滴加盐酸:2H++CO32-═CO2↑+H2O |
| B、向FeCl3溶液中通入H2S气体:Fe3++H2S═Fe2++S↓+2H+ |
| C、向碳酸氢钠溶液中滴加过量的澄清石灰水:HCO3-+Ca2++OH-═CaCO3↓+H2O |
| D、浓度均为0.1mol/L的硫酸氢铵与氢氧化钠两种溶液等体积混合:NH4++HSO4-+2OH-═SO42-+NH3↑+2H2O |
某同学将一小块金属钠投入到硫酸铜溶液中,通过此实验不能证明下列性质中的( )
| A、钠比水轻但比煤油重 |
| B、钠的熔点较低 |
| C、钠与水反应时要放出热量 |
| D、钠与水反应后溶液呈碱性 |
卤素单质的性质与F2>Cl2>Br2>I2的变化规律不相符的是( )
| A、与氢气反应的剧烈程度 |
| B、气态氢化物的稳定性 |
| C、单质还原性的强弱 |
| D、与水反应的剧烈程度 |
下列变化不属于化学变化的是( )
| A、次氯酸钠使有色布条褪色 |
| B、氯水使用色花辨褪色 |
| C、活性炭使红墨水褪色 |
| D、H2O2水溶液使染料褪色 |
设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A、7.8g Na2O2所含的阴离子数目为2NA |
| B、在熔融状态下,lmol KHSO4完全电离出的阳离子数目为2NA |
| C、14g乙烯和丙烯的混和气体中共含有3NA对共用电子对 |
| D、将分子总数为NA的NH3和HCl的混合气体置于标准状况下,其体积为约22.4L |