题目内容
18.对于下列反应的反应类型的判断,正确的是( )| A. | CO2+H2O=H2CO3分解反应 | |
| B. | Cu(OH)2$\frac{\underline{\;△\;}}{\;}$CuO+H2O 化合反应 | |
| C. | Fe2O3+3CO$\frac{\underline{\;△\;}}{\;}$2Fe+3CO2 置换反应 | |
| D. | NaCl+AgNO3=AgCl↓+NaNO3复分解反应 |
分析 两种或多种物质生成一种物质的反应为化合反应;
一种物质生成两种或多种物质的反应为分解反应;
一种单质和一种化合物反应生成另外的单质和化合物的反应为置换反应;
两种化合物相互交换成分生成另外的两种化合物的反应为复分解反应.
解答 解:A.该反应由两种物质生成一种物质,所以属于化合反应,故A错误;
B.该反应由一种物质生成两种物质,所以属于分解反应,故B错误;
C.该反应中反应物没有单质,生成物中有单质,所以不属于置换反应,故C错误;
D.该反应由两种化合物相互交换成分生成另外的两种化合物,属于复分解反应,故D正确,
故选D.
点评 本题考查化学基本反应类型的判断,根据概念判断即可,题目难度不大,学习中注意相关基础知识的积累.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
8.下列化学用语正确的是( )
| A. | 甲烷的球棍模型: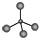 | B. | 羟基的电子式: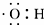 | ||
| C. | 乙醛的结构式:CH3CHO | D. | 乙酸的结构简式C2H4O2 |
9.在120℃时,1体积甲烷和丁烯的混合物与4体积O2在密闭容器中充分燃烧,只生成水和二氧化碳,反应后恢复到原温度,压强增加为原来的1.1倍,则混合气体中丁烯的体积分数是( )
| A. | 20% | B. | 40% | C. | 50% | D. | 9 5% |
3.现有稀盐酸、氢氧化钡溶液、氯化钠溶液三种无色溶液,小丽认为可用下列四种试剂进行一次性鉴别,你觉得不可行的是( )
| A. | 无色酚酞溶液 | B. | pH试纸 | C. | Na2CO3溶液 | D. | 紫色石蕊溶液 |
10.下列微粒中第一、第二层电子总和等于其第三、第四层电子总和的是( )
| A. | K | B. | Ca | C. | Mg | D. | S |
8.下列分子或离子在指定的分散系中能大量共存的一组是( )
| A. | 硝酸钠溶液:H+、Fe3+、SO42-、CH3COOH | |
| B. | 烧碱溶液:K+、HSO3-、NO3-、NH3•H2O | |
| C. | 空气:HCl、CO2、SO2、NO | |
| D. | 氢氧化铁胶体:H+、K+、S2-、Br- |
 常见金属X,有下列关系图,根据图示回答:
常见金属X,有下列关系图,根据图示回答: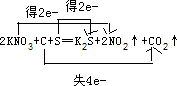 .
.