题目内容
11.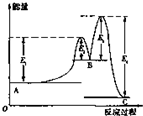 某反应由两步反应A?B?C构成,它的反应能量变化曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )
某反应由两步反应A?B?C构成,它的反应能量变化曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )| A. | A→C的反应为吸热反应 | B. | 三种物质中B最不稳定 | ||
| C. | 加入催化剂,E1、E2、E3、E4均不变 | D. | A→C反应的△H=E1-E2 |
分析 A→B的反应,反应物总能量小于生成物总能量,反应吸热,B→C的反应,反应物的总能量大于生成物总能量,反应为放热反应,结合能量的高低解答该题.
解答 解:A.A→C的反应为放热反应,故A错误;
B.物质的总能量越低,越稳定,C最稳定,B最不稳定,故B正确;
C..加入催化剂,只改变反应的活化能,即E1、E2、E3、E4均改变,不改变反应热,故C错误;
D.整个反应中△H=(E1-E2)+(E2-E3)-E4=E1-E3-E4,故D错误,故选B.
点评 本题考查化学反应与能量变化,题目难度不大,注意把握物质的总能量与反应热的关系,易错点为D,注意把握反应热的计算.

练习册系列答案
相关题目
1.下列叙述中,错误的是( )
| A. | 1mol的任何气体中都含有6.02×1023个分子 | |
| B. | 12g12C中含有6.02×1023个碳原子 | |
| C. | 1mol水中含有6.02×1023个氢原子 | |
| D. | 物质的量相等的CO和CO2所含的C原子个数也相等 |
2.氯化铜的水溶液为淡蓝色,当加入浓盐酸后,溶液就变成黄绿色,这种颜色的变化是由下列可逆反应引起的:
[Cu(H2O)4]2+(淡蓝色)+4Cl-?[CuCl4]2-(黄绿色)+4H2O,下列方法能使溶液变成淡蓝色的是( )
[Cu(H2O)4]2+(淡蓝色)+4Cl-?[CuCl4]2-(黄绿色)+4H2O,下列方法能使溶液变成淡蓝色的是( )
| A. | 加压 | B. | 加入NaCl溶液 | C. | 加AgNO3溶液 | D. | 加盐酸 |
19.下列不能用勒沙特列原理解释的是( )
| A. | 高压条件有利于合成氨反应 | |
| B. | 棕红色NO2加压后颜色先变深后变浅 | |
| C. | SO2催化氧化成SO3的反应,往往需要使用催化剂 | |
| D. | 增加氧气的量有利于SO2催化氧化成SO3 |
16.下列叙述正确的是( )
| A. | 已知反应:2H2O2$\frac{\underline{\;催化剂\;}}{\;}$O2↑+2H2O,反应过程中过氧化氢的物质的量浓度变化如表所示:
| |||||||||||||
| B. | 向Zn与盐酸的反应体系中补加盐酸化学反应速率一定加快 | |||||||||||||
| C. | 恒容密闭容器中发生反应:N2(g)+3H2(g)?2NH3(g),当反应达到平衡后,向体系中通入N2,NH3的体积分数一定增加 | |||||||||||||
| D. | 在一体积可变密闭容器中进行反应:CO(g)+2H2(g)?CH3OH(g),当反应达到平衡后,在保证H2浓度不变的前提下,向容器中通入H2平衡不移动 |
20.100mL浓度为2mol/L的盐酸跟略过量的锌片反应,为减慢反应速率,又不影响生成氢气的总量,可采用的方法是( )
| A. | 加入适量的6mol/L的盐酸 | B. | 加入数滴氯化铜溶液 | ||
| C. | 加入适量醋酸钠溶液 | D. | 加入适量的硝酸钾溶液 |
1.铁和下列物质反应,能生成+3价化合物的是( )
①O2 ②S ③HCl ④CuCl2 ⑤HNO3 ⑥溴 ⑦H2O.
①O2 ②S ③HCl ④CuCl2 ⑤HNO3 ⑥溴 ⑦H2O.
| A. | ①②⑤ | B. | ①⑥ | C. | ①⑤⑥⑦ | D. | ①⑤⑥ |
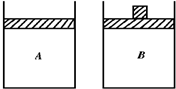 有两只相同的密闭容器A和B,A保持恒容,B保持恒压.起始时向这两只容器中分别充入等量的、物质的量比为4:5的NH3与O2的混合气体,并使A和B容积相等(如图所示),在保持500℃的条件下使之发生4NH3(g)+5O2(g)?4NO(g)+6H2O反应.填写下列空格:
有两只相同的密闭容器A和B,A保持恒容,B保持恒压.起始时向这两只容器中分别充入等量的、物质的量比为4:5的NH3与O2的混合气体,并使A和B容积相等(如图所示),在保持500℃的条件下使之发生4NH3(g)+5O2(g)?4NO(g)+6H2O反应.填写下列空格: