题目内容
2.氯化铜的水溶液为淡蓝色,当加入浓盐酸后,溶液就变成黄绿色,这种颜色的变化是由下列可逆反应引起的:[Cu(H2O)4]2+(淡蓝色)+4Cl-?[CuCl4]2-(黄绿色)+4H2O,下列方法能使溶液变成淡蓝色的是( )
| A. | 加压 | B. | 加入NaCl溶液 | C. | 加AgNO3溶液 | D. | 加盐酸 |
分析 使溶液变成淡蓝色,采取的操作使溶液中[Cu(H2O)4]2+浓度增大,即使平衡向逆反应方向移动,根据勒夏特列原理,只有通过减小Cl-浓度才能达到这种移动,据此分析.
解答 解:使溶液变成淡蓝色,采取的操作使溶液中[Cu(H2O)4]2+浓度增大,即使平衡向逆反应方向移动,根据勒夏特列原理,只有通过减小Cl-浓度才能达到这种移动.
A、该反应在溶液中进行,所以加压平衡不移动,故A错误;
B、加入NaCl溶液,即增大氯离子浓度,平衡向右移动,故B错误;
C、加入AgNO3溶液,银离子和氯离子结合生成氯化银沉淀,溶液中Cl-浓度浓度减小,平衡逆向进行,使黄绿色氯化铜溶液向蓝色转化,故C正确;
D、加入食盐晶体,溶液中Cl-浓度浓度增大,平衡向右移动,故D错误.
故选C.
点评 本题考查平衡的移动,难度中等,可以借助平衡常数理解稀释对平衡的影响.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
10.下列说法错误的是( )
| A. | 氯气的摩尔质量是71 g/mol | |
| B. | 通过树状分类法可把硝酸和硫酸分入强酸,把纯碱分入正盐 | |
| C. | 酸性的雨水都是酸雨,酸雨的PH小于7 | |
| D. | 1mol CO2的质量是44 g |
7.厨房中的化学知识很多,下面是有关厨房中的常见操作或者常见现象,其中发生的变化不属于氧化还原反应的是( )
| A. | 用活性炭除去冰箱中的异味 | B. | 燃烧液化石油气为炒菜提供热量 | ||
| C. | 食物长时间放置后变质腐败 | D. | 烧菜用过的铁锅出现红棕色斑迹 |
14.能在水溶液中大量共存的一组离子是( )
| A. | Ba2+、K+、OH-、SO42- | B. | Fe3+、NO3-、Na+、OH- | ||
| C. | H+、Na+、Cl-、SO42- | D. | K+、SO42-、HCO3-、H+ |
11.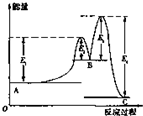 某反应由两步反应A?B?C构成,它的反应能量变化曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )
某反应由两步反应A?B?C构成,它的反应能量变化曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )
 某反应由两步反应A?B?C构成,它的反应能量变化曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )
某反应由两步反应A?B?C构成,它的反应能量变化曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )| A. | A→C的反应为吸热反应 | B. | 三种物质中B最不稳定 | ||
| C. | 加入催化剂,E1、E2、E3、E4均不变 | D. | A→C反应的△H=E1-E2 |
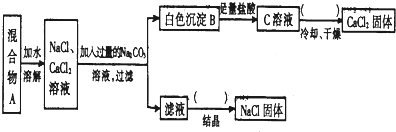
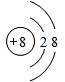 .
.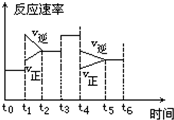 在一密闭体系中发生下列反应:N2+3H2?2NH3 △H<0,如图是某一时间段中反应速率与反应进程的曲线关系图:
在一密闭体系中发生下列反应:N2+3H2?2NH3 △H<0,如图是某一时间段中反应速率与反应进程的曲线关系图: