题目内容
【题目】砷是第ⅤA族元素,黄砷(As4)是砷元素的一种单质,其分子结构与白磷(P4)相似。下列关于黄砷和白磷的叙述正确的是()
A.黄砷和白磷分子中共价键的键角均为109.5o
B.黄砷分子中共价键的键能大于白磷分子
C.黄砷分子的极性大于白磷分子
D.黄砷的熔点高于白磷
【答案】D
【解析】
A.黄砷和白磷分子中共价键的键角均为60°,故A错误;
B.原子半径As>P,键长越大,键能越小,黄砷分子中共价键的键能小于白磷分子,故B错误;
C.黄砷和白磷分子均为非极性分子,分子极性相同,故C错误;
D.形成的晶体都为分子晶体,相对分子质量越大,分子间作用力越强,则熔点越高,黄砷的熔点高于白磷,故D正确;
故选D。

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案
相关题目
【题目】某100mL溶液中含有的部分离子浓度大小如图所示,该溶液可能还含有Fe3+、Ba2+、H+、SO42﹣、CO32﹣ .
(1)为了进一步确认,对该溶液进行实验检测: 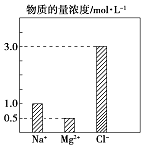
实验操作与现象 | 实验结论 | 判断理由 | |
步骤一 | 仔细观察坐标图 | 肯定无 | 肯定无该离子的理由 |
步骤二 | 该溶液呈无色、透明、均一状态 | 肯定无 | 肯定无该离子的理由 |
步骤三 | 加入足量BaCl2溶液,生成23.3g白色沉淀,再加稀硝酸,沉淀不消失 | 肯定有SO42﹣、H+;肯定无Ba2+ | 肯定有H+的理由 |
(2)实验操作的步骤三中称量沉淀前的实验操作步骤有:过滤、、灼烧、在干燥器中冷却.
(3)原溶液中H+物质的量浓度为mol/L.
(4)向溶液中加入NaHCO3溶液,反应的离子方程式为: .
(5)若向 100mL 该溶液中加入 1mol/L 的 Ba(OH)2溶液,恰好沉淀完全时加入的Ba(OH)2溶液体积为L.