题目内容
18.利用废镀锌皮制备磁性Fe3O4胶体粒子及副产物ZnSO4晶体的使用流程如下:已知:Zn及其化合物的性质与Al及其化合物的性质相似.
(1)用NaOH溶液处理废镀锌铁皮除溶解锌外,另一个作用是除去表面的油污.为缩短用NaOH溶液处理废镀锌铁皮的时间,可采用的措施是加热、将固体粉碎(答两条);
(2)加入适量H2O2溶液主要作用是氧化亚铁离子,溶液B中n(Fe2+):n(Fe3+)=1:2;
(3)在由溶液B制得Fe3O4胶体粒子的过程中,须缓慢滴加NaOH溶液并持续通入N2,持续通入N2的原因是防止Fe2+被氧化;
(4)请补充完整下列由溶液A获得副产品ZnSO4晶体的实验步骤:
①向溶液A中通入CO2气体,得到Zn(OH)2沉淀;②过滤、洗涤得到沉淀;③用适量的稀硫酸将沉淀完全溶解;④将溶液加热浓缩、冷却、洗涤、干燥即可得到产品.
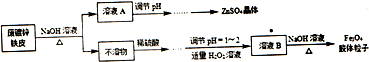
分析 废旧镀锌铁皮加入氢氧化钠溶液中反应,锌溶解生成偏锌酸钠和氢气,铁不溶解,过滤得到滤液A为Na2ZnO2,不溶物为Fe,溶液A调节pH使溶液中ZnO22-转化为Zn(OH)2沉淀,再经过抽滤、洗涤、干燥,灼烧得到ZnO.不溶物Fe中加入硫酸,反应生成硫酸亚铁,调节溶液PH=1~2,并加入适量过氧化氢,氧化部分亚铁离子为铁离子,得到含Fe2+、Fe3+的B溶液,再加入氢氧化钠溶液,加热分解生成四氧化三铁胶体粒子.
(1)根据Zn及化合物的性质与Al及化合物的性质相似,Zn也能和氢氧化钠溶液反应,氢氧化钠溶液起到溶解镀锌层和去除油污作用,为缩短用NaOH溶液处理废镀锌铁皮的时间,可以加热、将固体粉碎;
(2)H2O2具有氧化性,能将亚铁离子氧化;Fe3O4可以看做FeO•Fe2O3,故溶液B中n(Fe2+):n(Fe3+)=1:2,
(3)持续通入N2,防止Fe2+被氧化;
(4)向溶液A中通入CO2气体,得到Zn(OH)2沉淀,然后过滤、洗涤沉淀,用适量的稀硫酸将沉淀完全溶解,将溶液加热浓缩、冷却、洗涤、干燥即可得到ZnSO4晶体.
解答 解:废旧镀锌铁皮加入氢氧化钠溶液中反应,锌溶解生成偏锌酸钠和氢气,铁不溶解,过滤得到滤液A为Na2ZnO2,不溶物为Fe,溶液A调节pH使溶液中ZnO22-转化为Zn(OH)2沉淀,再经过抽滤、洗涤、干燥,灼烧得到ZnO.不溶物Fe中加入硫酸,反应生成硫酸亚铁,调节溶液PH=1~2,并加入适量过氧化氢,氧化部分亚铁离子为铁离子,得到含Fe2+、Fe3+的B溶液,再加入氢氧化钠溶液,加热分解生成四氧化三铁胶体粒子.
(1)根据Zn及化合物的性质与Al及化合物的性质相似,Zn也能和氢氧化钠溶液反应,氢氧化钠溶液起到溶解镀锌层和去除油污作用,为缩短用NaOH溶液处理废镀锌铁皮的时间,可以加热、将固体粉碎;
故答案为:除去表面的油污;加热、将固体粉碎;
(2)H2O2具有氧化性,能将亚铁离子氧化;Fe3O4可以看做FeO•Fe2O3,故溶液B中n(Fe2+):n(Fe3+)=1:2,
故答案为:氧化亚铁离子、1:2;
(3)持续通入N2,防止Fe2+被氧化,故答案为:防止Fe2+被氧化;
(4)向溶液A中通入CO2气体,得到Zn(OH)2沉淀,然后过滤、洗涤沉淀,用适量的稀硫酸将沉淀完全溶解,将溶液加热浓缩、冷却、洗涤、干燥即可得到ZnSO4晶体;
故答案为:过滤;用适量的稀硫酸将沉淀完全溶解.
点评 本题以“废旧镀锌铁皮可制备磁性Fe3O4胶体粒子及副产物ZnO”为载体,考查实验基本操作和技能,涉及标准溶液的配制、对信息的利用、实验条件的控制等,试题难度中等,是对学生综合能力的考查,需要学生基本知识的基础与分析问题、解决问题的能力.

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案| A. | 28g N2、N2O、N2O4的混合气体含有氮原子数为2NA | |
| B. | 质量均为7.8 g Na2S、Na2O2的固体中含有的阴离子数均为0.1NA | |
| C. | 0.5 mol•L-1的乙酸溶液中,乙酸分子的数目小于0.5NA | |
| D. | 78g苯分子中含有碳碳双键数为3 NA |
| A. | 若生成物C和D分别为盐和水,则该反应一定是中和反应 | |
| B. | 若A和C是单质,B和D是化合物,则该反应一定是置换反应 | |
| C. | 若A是可溶性碱,B是可溶性盐,则C和D不可能是两种沉淀 | |
| D. | 若A是可溶性碱,B是可溶性盐,则C和D一定是另一种碱和另一种盐 |
②N2(g)+2O2(g)═2NO2(g)△H=+67.8kJ•mol-1
③N2(g)+3H2(g)═2NH3(g)△H=-92.0kJ•mol-1
则4NH3(g)+7O2(g)═4NO2(g)+6H2O(g)△H=XkJ•mol-1中X的值是( )
| A. | -1131.2 | B. | -647.6 | C. | -507.8 | D. | -323.8 |
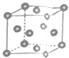
| A. | 只有金属钋原子采用这种堆积方式 | B. | 这种堆积方式中,配位数为8 | ||
| C. | 这是金属晶体的一种最密堆积方式 | D. | 这种堆积方式的空间利用率较低 |
2H2O2(l)=2H2O(l)+O2 (g)△H=-196.46kJ•mol-1
H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.84kJ•mol-1
则H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的△H为( )
| A. | +319.68kJ•mol-1 | B. | +259.7kJ•mol-1 | C. | -319.68kJ•mol-1 | D. | -259.7kJ•mol-1 |

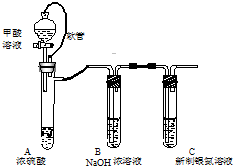 银氨溶液可用于检测CO气体,实验室研究的装置如图:
银氨溶液可用于检测CO气体,实验室研究的装置如图: .
.