题目内容
【题目】1999年1月,俄美科学家联合小组宣布合成了114号元素的一种同位素原子,其中子数为184,有关该元素和同位素原子的叙述中不正确的是( )
A.该原子位于元素周期表第七周期第![]() 族
族
B.该元素为金属,性质与![]() 相似
相似
C.该元素相对原子质量是298
D.该元素主要化合价为![]() 和
和![]()
【答案】C
【解析】
根据每周期元素的种数,可知每周期最后一种稀有气体元素的原子序数分别是:2、10、18、36、54、86、118,则114号元素在118号的左边,根据元素周期表中周期和族的划分,114号元素位于第七周期ⅣA族,据此分析解答。
A.由上述分析可知,该元素处于第七周期ⅣA族,故A正确;
B.该元素处于第七周期ⅣA,处于碳族,同主族自上而下金属性增强,同族的Pb为金属元素,故该元素为金属元素,与Pb的化学性质相似,故B正确;
C.质子数+中子数=质量数,质量数为298,该原子的近似相对原子质量为298,不是元素的近似相对原子质量,故C错误;
D.碳族元素的主要化合价为![]() 和
和![]() 价,故D正确;
价,故D正确;
故选C。

 快捷英语周周练系列答案
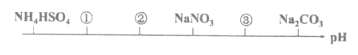
快捷英语周周练系列答案【题目】砂质土壤分析中常用KarlFischer法是测定其中微量水含量,该方法原理是I2和SO2反应定量消耗水(假设土壤中其他成分不参加反应),据此回答下列问题:
(1)写出该反应的化学反应方程式:________________________。
步骤①:消耗反应样品中的水
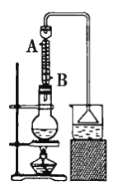
下图是某同学在实验室模拟KarlFischer法的实验装置图:
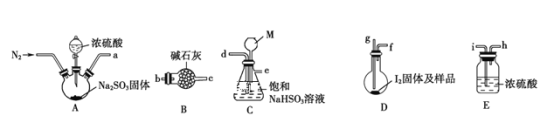
(2)装置连接的顺序为a__________(填接口字母顺序);M仪器的名称为__________,其在实验过程中的作用是__________________________。
(3)操作步骤①:连接装置并检查装置气密性,装入药品,_________________;关闭弹簧夹,打开分液漏斗活塞;反应结束后,关闭分液漏斗活塞,继续通入N2,取下D装置;步骤②:测定剩余的碘时,向反应后的D装置加入蒸馏水,过滤,充分洗涤滤渣,并合并洗涤液和滤液,将其配成250.00mL溶液,取25.00mL用0.20mol·L-1Na2S2O3标准液滴定剩余的碘单质,已知反应如下:2S2O![]() +I2=S4O
+I2=S4O![]() +2I-。
+2I-。
(4)Na2S2O3标准液应装在________(填“酸式”“碱式”)滴定管中;上述操作中,合并洗涤液和滤液的目的是________________________________。
(5)滴定实验重复四次得到数据如下:
实验 | 1 | 2 | 3 | 4 |
消耗的标准液的体积/mL | 18.37 | 20.05 | 19.95 | 20.00 |
①若实验开始时,向D装置中加入10.00g土壤样品和10.16gI2(已知I2过量),则样品土壤中水的含量为________%(计算结果保留小数点后一位)。
②若Na2S2O3标准液已部分氧化变质,则水含量测定结果将________(填“偏高”“偏低”或“不变”)。