题目内容
11.Cu(NO3)2是重要的化工原料.回答下列工业生产和化学实验中的几个问题.(1)实验室欲制备0.3mol Cu (NO3)2晶体,甲、乙两同学分别设计实验方案如下:
甲:Cu$\stackrel{稀H_{3}NO_{3}}{→}$Cu(NO3)乙:Cu$\stackrel{O_{2}}{→}$CuO$\stackrel{稀H_{3}NO_{3}}{→}$Cu(NO3)
①从绿色化学的角度分析,乙同学的方案更合理,此同学可节约2mol/L的稀硝酸100mL;
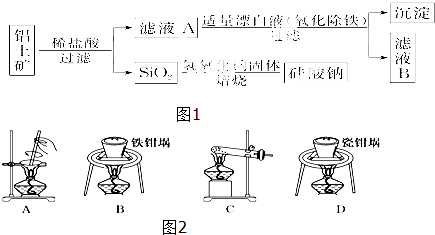
②乙同学实验时通入O2的速率不宜过大,为便于观察和控制产生O2的速率,宜选择如图A、B、C中B方案(填字母序号).
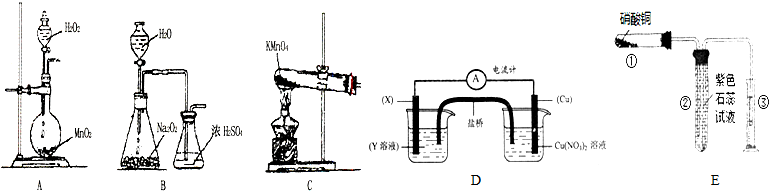
③有下述装置(图D),当装置电路中通过2mol电子时,Cu电极(填编号)c.
(a)增重64g (b)减重64g (c)可能增重64g,也可能减重64g
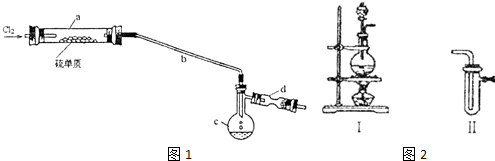
(2)①某校化学兴趣小组的同学对硝酸铜的受热分解进行探究.他们设计了如图D装置加热Cu(NO3)2固体(加热及夹持装置未画出).加热过程发现:装置①中的固体逐渐变为黑色;装置②中有气泡产生,但在上升的过程中消失;石蕊试液逐渐变为红色,液体几乎不被压至装置③中.请写出Cu(NO3)2受热分解的化学方程式:2Cu(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+4NO2↑+O2↑;
②在装置中①试管的橡皮塞最好用锡箔包住,原因是NO2气体会腐蚀橡胶.
分析 (1)①评价实验方案要从反应的可操作性,生成物的性质,环保节能等方面分析,甲同学用Cu$\stackrel{稀H_{3}NO_{3}}{→}$Cu(NO3)的方法,制备0.3mol Cu (NO3)2晶体,消耗硝酸0.8mol,乙同学用Cu$\stackrel{O_{2}}{→}$CuO$\stackrel{稀H_{3}NO_{3}}{→}$Cu(NO3)的方法,制备0.3mol Cu (NO3)2晶体,消耗硝酸0.3mol,据此计算;
②实验时通入O2的速率不宜过大,为便于观察和控制产生O2的速率,分析装置可知,利用分液漏斗控制加入过氧化氢的量能达到要求;
③铜是负极发生氧化反应,电极反应式为:Cu-2e-=Cu2+,铜如果是正极,电极反应式为:Cu2++2e-=Cu;
(2)①装置②中也有气泡产生,但在上升的过程中消失,说明生成物有二氧化氮和氧气,装置①中的固体逐渐变为黑色,说明生成物有氧化铜,请然后根据质量守恒配平;
②NO2气体会腐蚀橡胶,所以在装置中①试管的橡皮塞最好用锡箔包住.
解答 解:(1)①评价实验方案要从反应的可操作性,生成物的性质,环保节能等方面分析,甲同学用Cu$\stackrel{稀H_{3}NO_{3}}{→}$Cu(NO3)的方法,制备0.3mol Cu (NO3)2晶体,消耗硝酸0.8mol,乙同学用Cu$\stackrel{O_{2}}{→}$CuO$\stackrel{稀H_{3}NO_{3}}{→}$Cu(NO3)的方法,制备0.3mol Cu (NO3)2晶体,消耗硝酸0.6mol,所以乙同学节约2mol/L的稀硝酸的体积为$\frac{0.8-0.6}{2}$L=100mL,
故答案为:乙;100;
②实验时通入O2的速率不宜过大,为便于观察和控制产生O2的速率,分析装置可知,利用分液漏斗控制加入过氧化氢的量能达到要求,装置B中生成的氧气通过浓硫酸可以干燥氧气,同时观察气体气泡冒出的速率控制生成氧气的速率,所以选择B装置;
故答案为:B;
③铜是负极发生氧化反应,电极反应式为:Cu-2e-=Cu2+,铜如果是正极,电极反应式为:Cu2++2e-=Cu,所以当电路中通过2mol电子时,Cu电极质量变化可能增重64g,也可能减重64g,故选c;
(2)①加热的是Cu(NO3)2.加热过程发现:装置②中也有气泡产生,但在上升的过程中消失,石蕊试液逐渐变为红色,液体几乎不被压至装置③中,说明二氧化氮、氧气恰好与水反应生成硝酸,装置①中的固体逐渐变为黑色,说明生成氧化铜,则方程式为:2Cu(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+4NO2↑+O2↑,
故答案为:2Cu(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+4NO2↑+O2↑;
②在装置中①试管的橡皮塞最好用锡箔包住,原因是NO2气体会腐蚀橡胶,故答案为:NO2气体会腐蚀橡胶.
点评 本题考查了物质成分探究实验和电化学的相关知识,题目涉及的知识点比较多,分析一个反应的可行性要从多方面分析,如从反应的可行性,环保安全,操作简便,经济节能方面考虑,本题难度较大.

 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案| A. | 碳酸氢铵溶液与足量氢氧化钠溶液反应 NH${\;}_{4}^{+}$+OH-=NH3•H2O | |
| B. | 向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ | |
| C. | 乙醛与银氨溶液在热水浴中的反应CH3CHO+2[Ag(NH3)2]++2OH-$\stackrel{△}{→}$CH3COO-+NH4++2Ag↓+3NH3+H2O | |
| D. | 苯酚钠溶液中通入少量的CO2 2C6H5O-+CO2+H2O→2C6H5OH+CO32- |
 溶液再生,其装置示意图如下:
溶液再生,其装置示意图如下: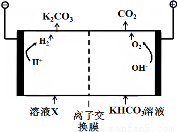
 H2O+CO2↑。
H2O+CO2↑。 O2(g)
O2(g) O2(g)
O2(g)
 生物燃料电池是一种利用微生物将化学能直接转化成电能的装置。已知某种甲醇微生物燃料电池中,电解质溶液为酸性,示意图如下:
生物燃料电池是一种利用微生物将化学能直接转化成电能的装置。已知某种甲醇微生物燃料电池中,电解质溶液为酸性,示意图如下: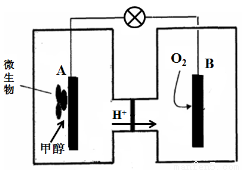 、
、