��Ŀ����
6��������أ�K2FeO4�������Ͷ��ˮ�����������������������ȶ����������������£�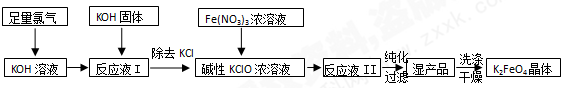
��ش���������
��1������ӦҺI�м���ϡ�����������壬д���䷴Ӧ�����ӷ���ʽCl-+Cl0-+2H+�T2H2O+Cl2����
��2�����ɡ���ӦҺ�����ӷ���ʽ��2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O��
��3��ʹ�ü���KClO��ԭ����K2FeO4�����������ȶ���
��4���ӡ���ӦҺ���з����K2FeO4����Ʒ��KCl������أ������ƣ����û�������D���������ᴿ������ĸ��ţ���A���� �� B���� Һ C���� �� D���� �� ��
��5�������K2FeO4����ϴ�ӵIJ��������������ˮϴ�ӣ�
��6����ҵ����1.98t K2FeO4������������Cl2�����ʵ���Ϊ15mol��
���� ����Cl2ͨ���KOH��Һ�У��¶ȵ�ʱ������ӦCl2+2OH-=Cl-+ClO-+H2O������ҺI�м���KOH��ʹ������ȫ��Ӧ���ҽ���Һת��Ϊ������Һ��ֻ�м��������´���������Ӳ��ܺ������ӷ���������ԭ��Ӧ���ɸ���������ӣ���ȥKCl�õ����Ե�KClOŨ��Һ������Ե�KClOŨ��Һ�м���90%��Fe��NO3��3��Һ��������Ӧ2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O���õ���ҺII�������õ�ʪ��Ʒ����ʪ��Ʒϴ�ӡ�����õ�����K2FeO4��
��1����������KOH��Ӧ�����Һ�ﺬ��Cl-��Cl0-�����Һ�еμ�ϡ�����ữ�������ӻᷢ��������ԭ��Ӧ����������
��2����ӦҺ���к���K2FeO4����֪����������ClO-����Fe3+�õ�2FeO42-�����ݵ����غ㡢����غ㼰ԭ���غ��д���˷�Ӧ�����ӷ���ʽ��
��3����K2FeO4��ˮ���Լ��ԣ�������Һ��������ˮ�⣬��֮���������»�ٽ�ˮ�⣻
��4���ɹ������̼��ۿ�֪���ӡ���ӦҺII���з����K2FeO4���и���ƷKNO3��KCl�����Ը��ݶ��ߵ��ܽ�Ȳ���ѡ����뷽ʽ��
��5�����������ˮϴ�Ӽ��ٲ�Ʒ�����������ӷ���
��6�����ݷ�ӦCl2+2OH-=Cl-+ClO-+H2O��2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O���ɵù�ϵʽ2K2FeO4��3Cl2�����ݹ�ϵʽ�ɼ�������������ʵ�����
��� �⣺��1����ӦҺI��Cl-��Cl0-�����������·������з�Ӧ�������������ӷ�Ӧ����ʽΪCl-+Cl0-+2H+�T2H2O+Cl2�����ʴ�Ϊ��Cl-+Cl0-+2H+�T2H2O+Cl2����
��2�����ݷ�����֪��Fe��NO3��3��Һ�����KClO��Һ��Ӧ���ɸ�����غ��Ȼ��أ���Ӧ�Ļ�ѧ����ʽΪ2Fe��NO3��3+3KClO+10KOH=2K2FeO4+3KCl+6KNO3+5H2O��
��Ӧ�����ӷ�Ӧ����ʽΪ2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O���ʴ�Ϊ��2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O��
��3��K2FeO4�����������ȶ���Ϊ�˵õ��ȶ���Ŀ����ף�Ӧѡ��ʹ�ü���KClO���ʴ�Ϊ��K2FeO4�����������ȶ���
��4���ɹ������̼��ۿ�֪���ӡ���ӦҺII���з����K2FeO4���и���ƷKNO3��KCl�����ݶ��ߵ��ܽ�����¶ȱ仯�����ѡ�����ؽᾧ�ķ������з��룬
�ʴ�Ϊ������أ�D��
��5�������������ˮϴ�Ӳ�Ʒ�������Ʒ�ܽ���ʧ��ͬʱ������ӷ������ڸ���ʴ�Ϊ�������������ˮϴ�ӣ�
��6�����ݷ�ӦCl2+2OH-=Cl-+ClO-+H2O��2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O���ɵù�ϵʽ2K2FeO4��3Cl2��1.98kg K2FeO4�����ʵ���Ϊ10mol�����ݹ�ϵʽ��֪���������ʵ���Ϊ15mol���ʴ�Ϊ��15��
���� ���⿼�����ʵķ�����ᴿ�����ؿ���ѧ������������������˼ά�������ԣ��漰������ԭ��Ӧ����ʽ����ƽ�����ӷ���ʽ����д����������Ϸ������ʷ������̣�֪��ÿһ�������ķ�Ӧ��������������Ŀ�ѶȲ���

 ��ѧ�����ϵ�д�
��ѧ�����ϵ�д� �·Ƿ��̸����100��ϵ�д�
�·Ƿ��̸����100��ϵ�д�ʵ��Ŀ�ģ�֤��Һ��ʯ�����к���C��HԪ�أ�
ʵ����Ʒ�������ƿ��������С�ձ�������ʯ��ˮ
| ʵ�鲽�� | ʵ������ | ���� |
| ��1����ȼҺ��ʯ���� ��2�����������С�ձ����ڻ����Ϸ� | �����ձ��ڱ���ˮ�� | ֤��������Ԫ�� |
| ��3����պ�г���ʯ��ˮ��С�ձ����ڻ����Ϸ� | �������ʯ��ˮ����� | ֤������̼Ԫ�� |
Ϊ���ᴿ��������(������Ϊ����),��ѡ�����Լ��ͷ��뷽������ȷ����( )
ѡ�� | ���ᴿ������(����) | �����Լ� | ���뷽�� |
A�� | H2O(Br2) | CCl4 | ��ȡ��Һ |
B�� | MgCl2��Һ(AlCl3) | Ũ��ˮ | ���� |
C�� | CO2(HCl) | ����Na2CO3��Һ | ϴ�� |
D�� | Si(Al) | NaOH��Һ | ���� |
 ʵʩ�Լ�����Դ�˷Ѻͽ��ͷ����ŷ�Ϊ�������ݵĽ��ܼ������ߣ���Ӧ��ȫ���������⡢������Դ��Լ�͡������Ѻ������ı�Ȼѡ������ҵ�ķ�չ������Ϲ��ҽ��ܼ��ŵ�����Ҫ����������ѧ֪ʶ������������⣺
ʵʩ�Լ�����Դ�˷Ѻͽ��ͷ����ŷ�Ϊ�������ݵĽ��ܼ������ߣ���Ӧ��ȫ���������⡢������Դ��Լ�͡������Ѻ������ı�Ȼѡ������ҵ�ķ�չ������Ϲ��ҽ��ܼ��ŵ�����Ҫ����������ѧ֪ʶ������������⣺��1����֪ij��Ӧ��ƽ�����ʽΪ��K=$\frac{{C��{H_2}��C��CO��}}{{C��{H_2}O��}}$����������ÿ����3gˮ������������22kJ����������÷�Ӧ���Ȼ�ѧ��ӦΪ��C��s��+H2O��g��
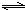 CO��g��+H2��g����H=+132kJ/mol
CO��g��+H2��g����H=+132kJ/mol��2����֪��һ���¶��£�
C��s��+CO2��g��?2CO��g��ƽ�ⳣ��K1��
CO��g��+H2O��g��?H2��g��+CO2��g��ƽ�ⳣ��K2��
C��s��+H2O��g��?CO��g��+H2��g�� ƽ�ⳣ��K3��
��K1��K2��K3֮��Ĺ�ϵ�ǣ�K3=K1��K2��
��3��ú����ͨ��ͨ���о���ͬ�¶���ƽ�ⳣ���Խ������ʵ�����⣮��֪�������һ����̼��ˮ�������뷴Ӧ��ʱ���ᷢ�����·�Ӧ��CO��g��+H2O��g��?H2��g��+CO2��g�����÷�Ӧƽ�ⳣ�����¶ȵı仯���±���ʾ��
| �¶�/�� | 400 | 500 | 800 |
| ƽ�ⳣ��K | 9.94 | 9 | 1 |
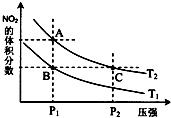
��4���Ӱ����������������ᣬ�˹������漰���������NO��NO2��N2O4�ȣ��Է�ӦN2O4��g��?2NO2��g����H��0���¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ����D��
A��A��C����ķ�Ӧ���ʣ�A��C
B��A��C�����������ɫ��A�Cdz
C��B��C����������ƽ����Է���������B��C
D����״̬B��״̬A�������ü��ȵķ���
E��A��C����Ļ�ѧƽ�ⳣ����A��C
��5��0.2mol/L��NaOH��0.4mol/L���������Һ�������Ϻ���Һ�и����ӵ����ʵ���Ũ�ȴӴ�С��˳����c��NO3-����c��NH4+����c��Na+����c��OH-����c��H+����
 ��
��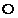 ������ͬԪ�ص�ԭ�ӡ�
������ͬԪ�ص�ԭ�ӡ�


 ��
��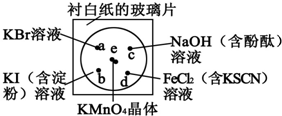 ijѧ�������в�����һ��ʵ�飺��һ���³İ�ֽ�IJ���Ƭ�IJ�ͬλ�÷ֱ�μ�Ũ��Ϊ0.1mol•L-1��KBr��KI����������Һ����NaOH������̪����FeCl2����KSCN����Һ��1�Σ�ÿ��Һ�α˴˷ֿ���Χ�ɰ뾶С�ڱ������Բ�Σ�����ͼ��ʾ������Բ�Ĵ�����2��֥������С��KMnO4���壬��KMnO4����μ�һ��Ũ���ᣬ��������������Ǻã�����֪2KMnO4+16HCl��Ũ���T2KCl+2MnCl2+5Cl2��+8H2O��
ijѧ�������в�����һ��ʵ�飺��һ���³İ�ֽ�IJ���Ƭ�IJ�ͬλ�÷ֱ�μ�Ũ��Ϊ0.1mol•L-1��KBr��KI����������Һ����NaOH������̪����FeCl2����KSCN����Һ��1�Σ�ÿ��Һ�α˴˷ֿ���Χ�ɰ뾶С�ڱ������Բ�Σ�����ͼ��ʾ������Բ�Ĵ�����2��֥������С��KMnO4���壬��KMnO4����μ�һ��Ũ���ᣬ��������������Ǻã�����֪2KMnO4+16HCl��Ũ���T2KCl+2MnCl2+5Cl2��+8H2O��