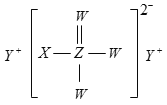题目内容
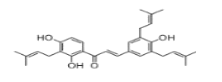
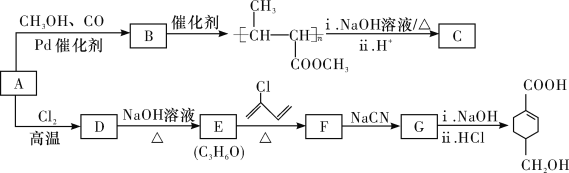
【题目】肉桂硫胺(Cinanserin)是上世纪70年代用于抗精神分裂症的药物,对冠状病毒3CL水解酶具有抑制作用,下图是其合成路线图。

已知以下信息:
①A为常见的烃,它对H2的相对密度为39
②2RCOOH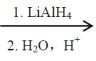 RCH2OH
RCH2OH
③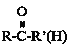 +HCN
+HCN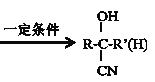
回答下列问题:
(1)A的名称__________;B的结构简式___________;肉桂硫胺中含氧官能团的名称__________。
(2)步骤①的反应方程式________________,其反应类型为_________。
(3)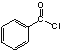 中共平面的原子最多________个。
中共平面的原子最多________个。
(4)M是C的同分异构体,符合下列条件的M有_______种。
①属于芳香族化合物。②能发生银镜反应。
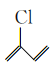
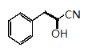
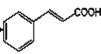
(5)参照题干,写出由![]() 制备
制备![]() 的流程图。_______。
的流程图。_______。
【答案】苯 ![]() 酰胺键
酰胺键 ![]() +CH3I
+CH3I![]()
![]() +HI 取代反应 14 4
+HI 取代反应 14 4 ![]()
![]()
![]()
![]()
![]()
![]()
![]()
【解析】
A经过①,发生取代反应生成B,B经过②,发生氧化反应得到C,C经过③得到 ,则C为苯甲酸,B为
,则C为苯甲酸,B为![]() ,A为苯,符合A为常见的烃,它对H2的相对密度为39。据此解答。
,A为苯,符合A为常见的烃,它对H2的相对密度为39。据此解答。
(1)根据分析可知,A为苯;B的结构简式为![]() ;肉桂硫胺由
;肉桂硫胺由![]() 为原料制得,含有胺,故中含氧官能团的名称酰胺键,故答案为:苯;
为原料制得,含有胺,故中含氧官能团的名称酰胺键,故答案为:苯;![]() ;酰胺键;
;酰胺键;
(2) 步骤①的反应方程式![]() +CH3I
+CH3I![]()
![]() +HI,为取代反应,故答案为:
+HI,为取代反应,故答案为:![]() +CH3I
+CH3I![]()
![]() +HI;取代反应;
+HI;取代反应;
(3)  中苯环上原子共平面,支链所连氧为碳氧双键也会共平面,所以最多有14个原子共平面,故答案为14;
中苯环上原子共平面,支链所连氧为碳氧双键也会共平面,所以最多有14个原子共平面,故答案为14;
(4) C为苯甲酸,满足①属于芳香族化合物,说明有苯环,②能发生银镜反应,要有醛基,苯甲酸有两个氧可以为醛基和酚羟基,有3中情况;还可以为甲酯,有一种情况,共有4种,故答案为:4;
(5)根据已知信息提示,![]() 可制得
可制得![]() ,
,![]() 可制得
可制得![]() ,
,![]() 可制得
可制得 ,
, 合成
合成 ,则合成路线为:
,则合成路线为:![]()
![]()
![]()
![]()
![]()
![]()

![]()
 ,故答案为:
,故答案为:![]()
![]()
![]()
![]()
![]()
![]()

![]()
 。
。

【题目】甲醇与水蒸气重整制氢可直接用于燃料电池。回答下列问题:
(1)已知:甲醇分解反应:CH3OH(g)![]() CO(g)+2H2(g) △H1=________ kJ·mol-1水蒸气变换反应:CO(g)+H2O(g)
CO(g)+2H2(g) △H1=________ kJ·mol-1水蒸气变换反应:CO(g)+H2O(g)![]() CO2(g)+H2(g) △H2=-41.20 kJ·mol-1,则CH3OH(g)+H2O(g)
CO2(g)+H2(g) △H2=-41.20 kJ·mol-1,则CH3OH(g)+H2O(g)![]() CO2(g)+3H2(g)△H3=+49.44kJ·mol-1。
CO2(g)+3H2(g)△H3=+49.44kJ·mol-1。
(2)科学家通过密度泛函理论研究甲醇与水蒸气重整制氢反应机理时,得到甲醇在Pd(Ⅲ)表面发生解离时四个路径与相对能量关系如图所示,其中附在Pd(Ⅲ)表面的物种用*标注。此历程中活化能最小的反应方程式为_________________________。
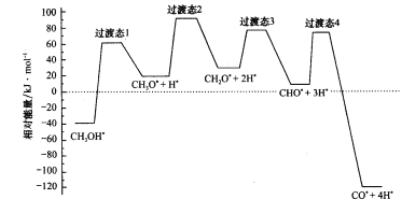
(3)在0.1MPa下,将总进料量1 mol且n(CH3OH):n(H2O)=1:1.3的混合气体充入一刚性密闭容器中反应。
①实验测得水煤气变换反应的速率随温度的升高明显下降,原因是__________。
②平衡时,测得CH3OH的含量在给定温度范围内极小,H2、H2O(g)、CO、CO2四种组分含量与反应温度关系如图所示,试解释a的含量约是c的含量3倍的原因__________。
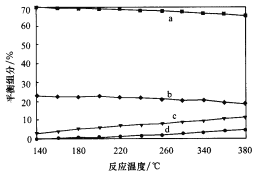
(4)297 K时,向密闭容器Ⅰ(体积为4L)和Ⅱ(体积为8L)中分别充入下列物质发生反应,
编号 | CO(mol) | H2(mol) | CH3OH(mol) |
Ⅰ | 4 | a | 0 |
Ⅱ | 4 | 4 | 4 |
达平衡时两个容器中c(H2)相等且c(H2)=0.5mol/L。则
①a=_____________。
②该温度时,Ⅰ中反应的K=___________。
③Ⅱ中按表格数据充入反应物此时反应的方向__________(填“正向进行”、“平衡”或“逆向进行”)。
【题目】根据下列实验操作和现象所得出的结论正确的是
选项 | 实验操作和现象 | 实验结论 |
A | 向20%蔗糖溶液中加入少量稀H2SO4,加热;再加入银氨溶液,水浴加热后未出现银镜 | 蔗糖未水解 |
B | 卤代烃Y与NaOH乙醇溶液共热后,加入足量稀硝酸,再滴加AgNO3溶液,产生白色沉淀 | 说明卤代烃Y中含有氯原子 |
C | 向浑浊的苯酚试液中加饱和Na2CO3溶液,试液变澄清且无气体产生 | 说明苯酚的酸性强于碳酸 |
D | 向鸡蛋清溶液中加入少量CuSO4溶液,出现浑浊 | 蛋白质发生了盐析 |
A. A B. B C. C D. D
【题目】CS2是一种常见溶剂,还可用于生产人造粘胶纤维等。回答下列问题:
(1)CS2与酸性KMnO4溶液反应,产物为CO2和硫酸盐,该反应中还原剂与氧化剂的物质的量之比为 _______(MnO4-被还原为Mn2+)
(2)甲烷硫磺法制取CS2的反应为CH4(g)+2S2(g)![]() CS2(g)+2H2S(g) △H。
CS2(g)+2H2S(g) △H。
① 在恒温恒容密闭容器中进行该反应时,能说明该反应已达到平衡状态的是_______(填字母)
A.v正(S2)=2v逆(CS2)
B.容器内气体的密度不再随时间变化
C.容器内气体的总压强不再随时间变化
D.单位时间内断裂C-H键数目与断裂H—S键数目相等
②已知下列键能数据:
共价键 | C—H | S=S | C=S | H—S |
律能/kJmol-1 | 411 | 425 | 573 | 363 |
该反应的△H _______kJmol-1
(3)在一密闭容器中,起始时向该容器中充入H2S和CH4且n(H2S):n(CH4)=2:1,发生反应:CH4(g) +2H2S(g)CS2(g) + 4H2(g)。0.1MPa时,温度变化对平衡时产物的物质的量分数的影响如图所示:
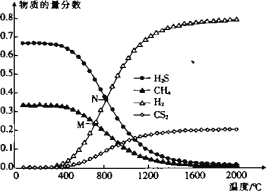
①该反应△H _______(填“>”或“<”)0。
②M点,H2S的平衡转化率为_______,为提高H2S的平衡转化率,除改变温度外,还可采取的措施是_______(列举一条)。
③N点,平衡分压p(CS2)=_______MPa,对应温度下,该反应的KP =_______(MPa)2。(KP为以分压表示的平衡常数)