题目内容
【题目】原电池原理的发现是贮能和供能技术的巨大进步。图所示原电池的说法正确的是
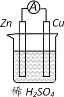
A.电子经锌片流向铜片
B.Cu为负极,Zn为正极
C.该装置能将电能转化为化学能
D.锌片上发生的反应为 2H++2e-=H2↑
【答案】A
【解析】
该装置为铜锌原电池,锌的活泼性大于铜,锌为负极,铜为正极,铜电极表面产生氢气,据此分析解答。
A.根据分析,锌为负极,铜为正极,原电池中电子由负极流向正极,则电子经外电路由锌片流向铜片,故A正确;
B.根据分析,锌为负极,铜为正极,故B错误;
C.该装置为原电池,原电池是将化学能转化为电能的装置,故C错误;
D.根据分析,锌为负极,负极上发生氧化反应,电极反应为:Zn-2e-=Zn2+;铜为正极,铜片上发生还原反应,产生氢气,电极反应为 2H++2e-=H2↑,故D错误;
答案选A。

【题目】甲、乙两同学用下图所示装置进行实验,探究硝酸与铁反应的产物。

文献记载:
I.在浓硝酸和活泼金属反应过程中,随着硝酸浓度的降低,其生成的产物有+4、+2、﹣3价等氮的化合物。
II.FeSO4+NOFe(NO)SO4(棕色) 。
III.NO2和NO都能被KMnO4氧化吸收。
甲的实验操作和现象记录如下:
实验操作 | 实验现象 |
(1)打开弹簧夹,通入一段时间某气体,关闭弹簧夹。 | |
(2)打开分液漏斗活塞,将浓硝酸缓慢滴入烧瓶中,关闭活塞。 | 无明显现象。 |
(3)加热烧瓶,反应开始后停止加热。 | ①A中有红棕色气体产生,一段时间后,气体颜色逐渐变浅; B中溶液变棕色; C中溶液紫色变浅。 ②反应停止后,A中有固体剩余。 |
请回答下列问题:
(1)为排除空气对实验的干扰,操作(1)中通入的气体可能是________________。
(2)滴入浓硝酸加热前没有明显现象的原因是__________________________。
(3)试写出加热烧瓶后A中有红棕色气体产生的化学方程式_______________。
(4)甲认为B中溶液变棕色是因为A中有NO生成,你认为甲的观点对吗_________(填正确或错误)?请结合方程式简述原因 ________________________________。
(5)检验是否生成﹣3价氮的化合物,应进行的实验操作是________________________。