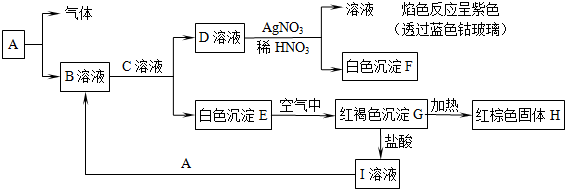
题目内容
2.已知重铬酸钾(K2Cr2O7)溶液中存在如下平衡:Cr2O7 2-(橙色)+H2O?2H++2CrO42- (黄色),①向2mL 0.1mol•L-1 K2Cr2O7溶液中滴入3滴6mol•L-1 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色.
②向2mL 0.1mol•L-1 酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O7 2-+14H++6Fe2+═2Cr3+(绿色)+6Fe3++7H2O.
下列分析正确的是( )
| A. | 实验①和②均能证明K2Cr2O7溶液中存在上述平衡 | |
| B. | 实验②能说明氧化性:Cr2O7 2->Fe3+ | |
| C. | 稀释K2Cr2O7溶液时,溶液中各离子浓度均减小 | |
| D. | CrO42- 和Fe2+在酸性溶液中可以大量共存 |
分析 A、溶液由橙色变为黄色,溶液由黄色变为橙色,说明加入酸碱发生平衡移动;
B、氧化剂的氧化性大于氧化产物分析判断;
C、稀释溶液,平衡状态下离子浓度减小,氢离子浓度减小,溶液中存在离子积,氢氧根离子浓度增大;
D、CrO42-具有氧化性,酸性溶液中氧化亚铁离子.
解答 解:A、加入氢氧化钠溶液,溶液由橙色变为黄色,说明平衡正向进行,加入硫酸溶液由黄色变为橙色,说明平衡逆向进行,说明加入酸碱发生平衡移动,实验①能证明K2Cr2O7溶液中存在上述平衡,实验②不能证明K2Cr2O7溶液中存在上述平衡,故A错误;
B、反应中Cr2O72-+14H++6Fe2+═2Cr3+(绿色)+6Fe3++7H2O,氧化剂的氧化性大于氧化产物,所以实验②能说明氧化性:Cr2O72->Fe3+,故B正确;
C、稀释K2Cr2O7溶液时,平衡状态下离子浓度减小,氢离子浓度减小,由离子积不变可知,氢氧根离子浓度增大,故C错误;
D、CrO42-具有氧化性,酸性溶液中氧化亚铁离子,CrO42-和Fe2+在酸性溶液中不可以大量共存,故D错误;
故选B.
点评 本题考查了盐类水解的分析应用,氧化还原反应的规律分析,平衡移动原理的理解应用,掌握基础是解题关键,题目难度中等.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
12.下列实验操作:①用50mL量筒量取5mL蒸馏水;②称量没有腐蚀性固体药品时,把药品放在托盘上称量;③倾倒液体时试剂不对准容器口;④块状药品都要用药匙取用;⑤固体药品用广口瓶保存.其中不正确的是( )
| A. | ①②③④ | B. | ③④ | C. | ②⑤ | D. | ①②④⑤ |
13.蒸发操作中必须用到蒸发皿,下列有关蒸发皿的操作中,不正确的是( )
| A. | 将蒸发皿放置在铁架台的铁圈上直接用酒精灯火焰加热 | |
| B. | 将蒸发皿放置在铁架台的铁圈上,并加垫石棉网加热 | |
| C. | 将蒸发皿放置在三脚架上直接用酒精灯火焰加热 | |
| D. | 将灼热的蒸发皿放置一段时间变凉后,放在冷水中冲洗 |
7.单质Ti的机械强度高,抗蚀能力强,有“未来金属”之称.工业上常用硫酸分解钛铁矿(FeTiO3)的方法来制取TiO2,再由TiO2制金属Ti.由TiO2制金属Ti的反应为:
①TiO2+2C+2Cl2 $\frac{\underline{\;高温\;}}{\;}$ TiCl4+2CO ②TiCl4+2Mg $\frac{\underline{\;高温\;}}{\;}$ 2MgCl2+Ti
则下列叙述正确的是( )
①TiO2+2C+2Cl2 $\frac{\underline{\;高温\;}}{\;}$ TiCl4+2CO ②TiCl4+2Mg $\frac{\underline{\;高温\;}}{\;}$ 2MgCl2+Ti
则下列叙述正确的是( )
| A. | 由反应①可知,Cl2是氧化剂,TiCl4是氧化产物 | |
| B. | 由反应①可知,可用CO在高温下把TiO2还原成Ti | |
| C. | 由反应②可知,若有24 g Mg参加反应,就可生成1 mol Ti | |
| D. | 由反应②可知,金属Mg的还原性比金属Ti的还原性强 |
12.下列表示对应化学反应的离子方程式正确的是( )
| A. | FeCl3溶液与Cu的反应:Cu+Fe3+═Cu2++Fe2+ | |
| B. | 向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- | |
| C. | 醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | NO2与水的反应:3NO2+H2O═2NO3-+NO+2H+ |
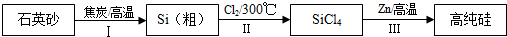
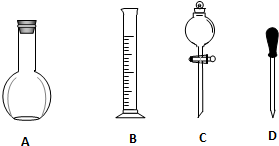 实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.
实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.