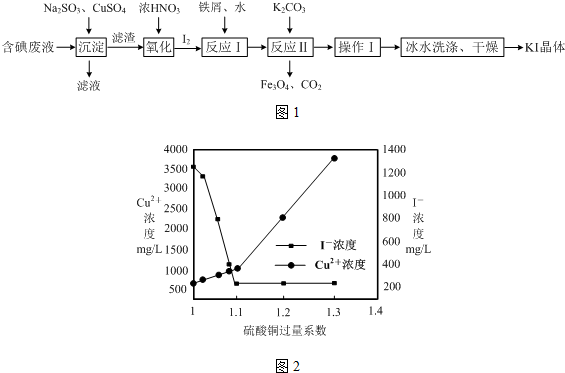
题目内容
17.硅是信息产业、太阳能电池光电转化的基础材料.锌还原四氯化硅是一种有着良好应用前景的制备硅的方法,该制备过程示意如下: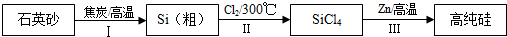
(1)硅元素位于元素周期表的第三周期ⅣA族.
(2)已知反应Ⅰ得到的粗硅中含有SiC,其中Si和SiC的物质的量之比为2:1.写出制造粗硅时的反应方程式3SiO2+7C$\frac{\underline{\;高温\;}}{\;}$2Si+SiC+6CO↑.SiC熔融时不导电,工业上常用作耐火和高温炉的材料,由此推知,它属于原子晶体.
(3)因为SiCl4遇水剧烈水解生成SiO2和一种酸,所以整个制备过程必须严格控制无水条件.在干燥Cl2时,从有利于充分干燥和操作安全的角度考虑,需将约90℃的潮湿氯气先冷却至12℃,然后再通入到浓H2SO4中.冷却的作用是使水蒸气冷凝,减少进入浓硫酸的水,保持浓硫酸持续的吸水性,同时降低放出的热量.
分析 (1)硅是14号元素在周期表中处于第三周期,第ⅣA族元素;
(2)已知反应Ⅰ得到的粗硅中含有SiC,其中Si和SiC的物质的量之比为2:1,而制造粗硅是碳和二氧化硅反应制,根据信息可知反应方程式为:3SiO2+7C$\frac{\underline{\;高温\;}}{\;}$2Si+SiC+6CO↑;SiC是原子晶体;
(3)使水蒸气冷凝,减少进入浓硫酸的水,保持浓硫酸持续的吸水性,同时降低放出的热量.
解答 解:(1)硅是14号元素在周期表中处于第三周期,第ⅣA族元素,故答案为:三;ⅣA;
(2)已知反应Ⅰ得到的粗硅中含有SiC,其中Si和SiC的物质的量之比为2:1,而制造粗硅是碳和二氧化硅反应制,根据信息可知反应方程式为:3SiO2+7C$\frac{\underline{\;高温\;}}{\;}$2Si+SiC+6CO↑,SiC是原子晶体;故答案为:3SiO2+7C$\frac{\underline{\;高温\;}}{\;}$2Si+SiC+6CO↑;原子;
(3)将约90℃的潮湿氯气先冷却至12℃,然后再通入浓H2SO4中,可使水蒸气冷凝,减少进入浓硫酸的水,保持浓硫酸持续的吸水性,同时降低放出的热量,
故答案为:使水蒸气冷凝,减少进入浓硫酸的水,保持浓硫酸持续的吸水性,同时降低放出的热量.
点评 本题以硅的制备为载体,考查硅及其化合物的性质、氧化还原反应和浓硫酸的性质、对操作的分析评价等,基本属于拼合型题目,需要学生具备扎实的基础,难度中等.

练习册系列答案
相关题目
7. 如图装置中,容器甲内充入0.1mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体.恒温下,容器甲中活塞缓慢由D向左移动,当移至C处时容器体积缩小至最小,为原体积的$\frac{9}{10}$,干燥管中物质的质量增加2.24g随着CO2的继续通入,活塞又逐渐向右移动.已知:2Na2O2+2CO2═2Na2CO3+O2 2NO+O2═2NO2 2NO2?N2O4(不考虑活塞的摩擦)下列说法中正确的是( )
如图装置中,容器甲内充入0.1mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体.恒温下,容器甲中活塞缓慢由D向左移动,当移至C处时容器体积缩小至最小,为原体积的$\frac{9}{10}$,干燥管中物质的质量增加2.24g随着CO2的继续通入,活塞又逐渐向右移动.已知:2Na2O2+2CO2═2Na2CO3+O2 2NO+O2═2NO2 2NO2?N2O4(不考虑活塞的摩擦)下列说法中正确的是( )
 如图装置中,容器甲内充入0.1mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体.恒温下,容器甲中活塞缓慢由D向左移动,当移至C处时容器体积缩小至最小,为原体积的$\frac{9}{10}$,干燥管中物质的质量增加2.24g随着CO2的继续通入,活塞又逐渐向右移动.已知:2Na2O2+2CO2═2Na2CO3+O2 2NO+O2═2NO2 2NO2?N2O4(不考虑活塞的摩擦)下列说法中正确的是( )
如图装置中,容器甲内充入0.1mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体.恒温下,容器甲中活塞缓慢由D向左移动,当移至C处时容器体积缩小至最小,为原体积的$\frac{9}{10}$,干燥管中物质的质量增加2.24g随着CO2的继续通入,活塞又逐渐向右移动.已知:2Na2O2+2CO2═2Na2CO3+O2 2NO+O2═2NO2 2NO2?N2O4(不考虑活塞的摩擦)下列说法中正确的是( )| A. | 活塞从D处移动到C处的过程中,通入CO2体积为2.24L(标准状况) | |
| B. | NO2转化为N2O4的转换率为20% | |
| C. | 活塞移至C处后,继续通入0.01mol CO2,此时活塞恰好回到D处 | |
| D. | 若改变干燥管中Na2O2的量,要通过调节甲容器的温度及通入CO2的量,使活塞发生从D到C,又从C到D的移动,则Na2O2的质量应大于1.56g |
8.工业生产水煤气的反应为:C(s)+H2O(g)?CO(g)+H2(g)△H=+131.4kJ•mol-1下列判断正确的是( )
| A. | 水煤气反应中,生成1molH2(g)吸收131.4 kJ热量 | |
| B. | CO(g)+H2(g)?C(s)+H2O(g)△H=+131.4kJ•mol-1 | |
| C. | 水煤气反应中生成1体积CO(g)吸收131.4 kJ热量 | |
| D. | 反应物能量总和大于生成物能量总和 |
12.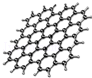 石墨烯是从石墨中剥离出来的,其结构如图所示.单层的石墨烯其厚度只有一个碳原子厚,被证实是世界上已经发现的最薄、最坚硬的物质,可制成电阻率最小的纳米材料.下列关于石墨烯的说法正确的是( )
石墨烯是从石墨中剥离出来的,其结构如图所示.单层的石墨烯其厚度只有一个碳原子厚,被证实是世界上已经发现的最薄、最坚硬的物质,可制成电阻率最小的纳米材料.下列关于石墨烯的说法正确的是( )
 石墨烯是从石墨中剥离出来的,其结构如图所示.单层的石墨烯其厚度只有一个碳原子厚,被证实是世界上已经发现的最薄、最坚硬的物质,可制成电阻率最小的纳米材料.下列关于石墨烯的说法正确的是( )
石墨烯是从石墨中剥离出来的,其结构如图所示.单层的石墨烯其厚度只有一个碳原子厚,被证实是世界上已经发现的最薄、最坚硬的物质,可制成电阻率最小的纳米材料.下列关于石墨烯的说法正确的是( )| A. | 石墨烯与金刚石互为同位素 | |
| B. | 从石墨中剥离得石墨烯需克服范德华力 | |
| C. | 石墨烯是高分子化合物 | |
| D. | 制成的纳米材料微粒直径在1nm~100nm,因此石墨烯纳米材料属于胶体 |
2.已知重铬酸钾(K2Cr2O7)溶液中存在如下平衡:Cr2O7 2-(橙色)+H2O?2H++2CrO42- (黄色),
①向2mL 0.1mol•L-1 K2Cr2O7溶液中滴入3滴6mol•L-1 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色.
②向2mL 0.1mol•L-1 酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O7 2-+14H++6Fe2+═2Cr3+(绿色)+6Fe3++7H2O.
下列分析正确的是( )
①向2mL 0.1mol•L-1 K2Cr2O7溶液中滴入3滴6mol•L-1 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色.
②向2mL 0.1mol•L-1 酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O7 2-+14H++6Fe2+═2Cr3+(绿色)+6Fe3++7H2O.
下列分析正确的是( )
| A. | 实验①和②均能证明K2Cr2O7溶液中存在上述平衡 | |
| B. | 实验②能说明氧化性:Cr2O7 2->Fe3+ | |
| C. | 稀释K2Cr2O7溶液时,溶液中各离子浓度均减小 | |
| D. | CrO42- 和Fe2+在酸性溶液中可以大量共存 |
9.下列说法不正确的是( )
| A. | 丁达尔现象可用于区别溶液与胶体,云、雾、墨水、有色玻璃均能产生丁达尔现象 | |
| B. | 原子吸收光谱仪可用于测定物质中的金属元素,红外光谱仪可用于测定化合物的官能团 | |
| C. | 安装煤炭燃烧过程的“固硫”装置,主要是为了提高煤的利用率 | |
| D. | 分子间作用力比化学键弱得多,但它对物质熔点、沸点、溶解度有较大影响 |
6.实验室需用480mL 0.10mol/L的CuSO4溶液,现选用500mL的容量瓶配制该溶液,下列方法可行的是( )
| A. | 称取8.0 g CuSO4,加入500 mL水 | |
| B. | 称取7.68 g CuSO4,加入480 mL水 | |
| C. | 称取12.5 g CuSO4•5H2O,加水配成500 mL溶液 | |
| D. | 称取12.0 g CuSO4•5H2O,加水配成480 mL溶液 |

 .
.