题目内容
12.下列实验操作:①用50mL量筒量取5mL蒸馏水;②称量没有腐蚀性固体药品时,把药品放在托盘上称量;③倾倒液体时试剂不对准容器口;④块状药品都要用药匙取用;⑤固体药品用广口瓶保存.其中不正确的是( )| A. | ①②③④ | B. | ③④ | C. | ②⑤ | D. | ①②④⑤ |
分析 ①量筒量取5mL蒸馏水应该选用10mL量筒;
②根据称量没有腐蚀性固体药品时的正确操作分析;
③应该试剂瓶口与容器口紧靠在一起;
④取块状固体一般用镊子取用;
⑤固体药品用广口瓶,液体用细口瓶.
解答 解:①用50mL量筒量取5mL蒸馏水,误差太大,应该用10mL量筒,故①错误;
②应在托盘上各放一张质量相同的纸片,以免污染药品,损坏托盘,故②错误;
③倾倒液体时,应使试剂瓶口与容器口紧靠在一起,故③错误;
④固体药品取用时,取用粉末状固体用药匙,块状固体一般用镊子,故④错误;
⑤为了便于取用药品,通常固体药品用广口瓶,液体用细口瓶盛放,故⑤正确;
故选A.
点评 本题考查了计量仪器的使用方法、药品的取用及保存方法、化学实验安全及事故处理,题目难度不大,要求学生熟练掌握常用仪器的使用方法、药品的正确取用和保存方法.

练习册系列答案
相关题目
7. 如图装置中,容器甲内充入0.1mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体.恒温下,容器甲中活塞缓慢由D向左移动,当移至C处时容器体积缩小至最小,为原体积的$\frac{9}{10}$,干燥管中物质的质量增加2.24g随着CO2的继续通入,活塞又逐渐向右移动.已知:2Na2O2+2CO2═2Na2CO3+O2 2NO+O2═2NO2 2NO2?N2O4(不考虑活塞的摩擦)下列说法中正确的是( )
如图装置中,容器甲内充入0.1mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体.恒温下,容器甲中活塞缓慢由D向左移动,当移至C处时容器体积缩小至最小,为原体积的$\frac{9}{10}$,干燥管中物质的质量增加2.24g随着CO2的继续通入,活塞又逐渐向右移动.已知:2Na2O2+2CO2═2Na2CO3+O2 2NO+O2═2NO2 2NO2?N2O4(不考虑活塞的摩擦)下列说法中正确的是( )
 如图装置中,容器甲内充入0.1mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体.恒温下,容器甲中活塞缓慢由D向左移动,当移至C处时容器体积缩小至最小,为原体积的$\frac{9}{10}$,干燥管中物质的质量增加2.24g随着CO2的继续通入,活塞又逐渐向右移动.已知:2Na2O2+2CO2═2Na2CO3+O2 2NO+O2═2NO2 2NO2?N2O4(不考虑活塞的摩擦)下列说法中正确的是( )
如图装置中,容器甲内充入0.1mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体.恒温下,容器甲中活塞缓慢由D向左移动,当移至C处时容器体积缩小至最小,为原体积的$\frac{9}{10}$,干燥管中物质的质量增加2.24g随着CO2的继续通入,活塞又逐渐向右移动.已知:2Na2O2+2CO2═2Na2CO3+O2 2NO+O2═2NO2 2NO2?N2O4(不考虑活塞的摩擦)下列说法中正确的是( )| A. | 活塞从D处移动到C处的过程中,通入CO2体积为2.24L(标准状况) | |
| B. | NO2转化为N2O4的转换率为20% | |
| C. | 活塞移至C处后,继续通入0.01mol CO2,此时活塞恰好回到D处 | |
| D. | 若改变干燥管中Na2O2的量,要通过调节甲容器的温度及通入CO2的量,使活塞发生从D到C,又从C到D的移动,则Na2O2的质量应大于1.56g |
17.在25℃时,某溶液中由水电离出的[H+]=1×10-12 mol•L-1,则该溶液的pH可能是( )
| A. | 12 | B. | 10 | C. | 6 | D. | 4 |
4.依据氧化还原反应:2Ag+(aq)+Cu(s)=2Ag(s)+Cu2+(aq)设计的原电池如图所示.下列说法正确的是( )


| A. | 银电极是负极 | B. | X电极是锌电极 | ||
| C. | 去掉盐桥电流计指针仍偏转 | D. | Y溶液为AgNO3溶液 |
1.用惰性电极电解物质的量浓度相同、体积比为3:1的CuSO4溶液和NaCl溶液的混合溶液,不可能发生的反应是( )
| A. | 2Cu2++2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+4H++O2↑ | B. | Cu2++2Cl-$\frac{\underline{\;通电\;}}{\;}$Cu+Cl2↑ | ||
| C. | 2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑ | D. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ |
2.已知重铬酸钾(K2Cr2O7)溶液中存在如下平衡:Cr2O7 2-(橙色)+H2O?2H++2CrO42- (黄色),
①向2mL 0.1mol•L-1 K2Cr2O7溶液中滴入3滴6mol•L-1 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色.
②向2mL 0.1mol•L-1 酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O7 2-+14H++6Fe2+═2Cr3+(绿色)+6Fe3++7H2O.
下列分析正确的是( )
①向2mL 0.1mol•L-1 K2Cr2O7溶液中滴入3滴6mol•L-1 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色.
②向2mL 0.1mol•L-1 酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O7 2-+14H++6Fe2+═2Cr3+(绿色)+6Fe3++7H2O.
下列分析正确的是( )
| A. | 实验①和②均能证明K2Cr2O7溶液中存在上述平衡 | |
| B. | 实验②能说明氧化性:Cr2O7 2->Fe3+ | |
| C. | 稀释K2Cr2O7溶液时,溶液中各离子浓度均减小 | |
| D. | CrO42- 和Fe2+在酸性溶液中可以大量共存 |
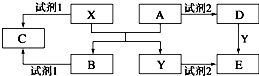 A、B、C、D、E是中学化学常见的5种化合物,其中A、B是氧化物.单质X、Y是生活中常见的金属,相关物质间的转化关系如图所示(部分反应物与产物已略去):
A、B、C、D、E是中学化学常见的5种化合物,其中A、B是氧化物.单质X、Y是生活中常见的金属,相关物质间的转化关系如图所示(部分反应物与产物已略去):