题目内容
【题目】Ⅰ.一研究性学习小组对某工业城市的空气污染进行了下列研究。
(1)小组一同学分析“空气质量日报”后初步得出结论,该城市空气污染的主要原因有:A.使用石油液化气 B.燃烧含硫煤 C.粉尘污染另一同学认为还有一个不可排除的原因是:D______。目前城市空气污染的主要有害成分是______ (用化学式表示)。
(2)空气污染形成酸雨.研究性学习小组对该市的雨水进行了采样与分析,刚采集时测得pH为4.82,放在烧杯中经2h后,再次测得pH为4.68.对此,你的合理的解释是______。
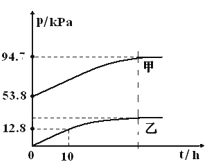
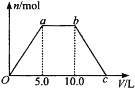
Ⅱ.在一密闭容器中发生反应 2NO2![]() 2NO+O2△H>0,反应过程中NO2的浓度随时间变化的情况如图所示,请回答:
2NO+O2△H>0,反应过程中NO2的浓度随时间变化的情况如图所示,请回答:
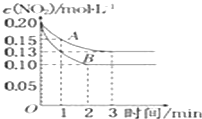
①依曲线A,反应在前3min内氧气的平均反应速率为______。
②若曲线A、B分别表示的是该反应在某不同条件下的反应情况,则此条件可能是______ (填“浓度”、“压强”、“温度”或“催化剂”).
(3)一定温度下,在密闭容器中N2O5可发生下列反应:
①2N2O5 (g) ![]() 4NO2 (g)+O2 (g)
4NO2 (g)+O2 (g)
②2NO2(g) ![]() 2NO(g)+O2 (g)若达平衡时,c(NO2)=0.4mol/L,c(O2)=1.3mol/L,
2NO(g)+O2 (g)若达平衡时,c(NO2)=0.4mol/L,c(O2)=1.3mol/L,
则反应②中NO2的转化率为______,N2O5 (g)的起始浓度应不低于______ mol/L。
【答案】机动车尾气污染 ![]() 等 雨水样品中的
等 雨水样品中的![]() 被空气中的氧气氧化为
被空气中的氧气氧化为![]()
![]() 温度
温度 ![]() 1
1
【解析】
(I)(1)城市中机动车多,排放的尾气中含有氮的氧化物等有害物质,会造成大气污染;目前城市空气污染的主要有害成分是二氧化硫等;
(2)雨水样品中的H2SO3被空气中的氧气氧化为H2SO4;
(Ⅱ)①根据v=![]() 计算v(NO2),再利用速率之比等于化学计量数之比计算v(O2);
计算v(NO2),再利用速率之比等于化学计量数之比计算v(O2);
②根据曲线及化学平衡原理解答;
(3)利用三段式结合转化率进行计算解答。
![]() 城市中机动车多,排放的尾气中含有氮的氧化物等有害物质,会造成大气污染;目前城市空气污染的主要有害成分是二氧化硫等;
城市中机动车多,排放的尾气中含有氮的氧化物等有害物质,会造成大气污染;目前城市空气污染的主要有害成分是二氧化硫等;
![]() 亚硫酸含有较强的还原性,雨水样品中的
亚硫酸含有较强的还原性,雨水样品中的![]() 被空气中的氧气氧化为
被空气中的氧气氧化为![]() ,酸性增强;
,酸性增强;
![]() Ⅱ
Ⅱ![]() 内
内![]() ,速率之比等于化学计量数之比,则
,速率之比等于化学计量数之比,则![]() ;
;
![]() 曲线A、B中
曲线A、B中![]() 的起始浓度相同,B曲线比A曲线反应速率快,且平衡时
的起始浓度相同,B曲线比A曲线反应速率快,且平衡时![]() 的浓度比A小,说明条件不同影响平衡移动,不能是催化剂,若为压强不同,应是B的压强高,平衡时
的浓度比A小,说明条件不同影响平衡移动,不能是催化剂,若为压强不同,应是B的压强高,平衡时![]() 浓度应比A的高,则不能为压强不同,而正反应为吸热反应,若温度不同,则B的温度高,升高温度,平衡正向移动,平衡时
浓度应比A的高,则不能为压强不同,而正反应为吸热反应,若温度不同,则B的温度高,升高温度,平衡正向移动,平衡时![]() 浓度应比A的低,则此条件可能是:温度不同;
浓度应比A的低,则此条件可能是:温度不同;
![]() 设
设![]() 中分解生成的
中分解生成的![]() 为
为![]() ,
,![]() 中分解的
中分解的![]() 为
为![]() ,则:
,则:
![]()
![]()
所以![]() ,解得
,解得![]() ,
,![]()
故![]() 中
中![]() 的转化率
的转化率![]() ,由于为可逆反应,故
,由于为可逆反应,故![]() 中
中![]() 不能完全分解,则其浓度应大于
不能完全分解,则其浓度应大于![]() ,即大于
,即大于![]() 。
。

【题目】化学中很多规律![]() 性质
性质![]() 都有其适用范围,下列根据其推出的结论正确的是( )
都有其适用范围,下列根据其推出的结论正确的是( )
选项 | 规律 | 结论 |
A | 主族元素最高正化合价等于族序数 | 第ⅦA族元素最高正价都是+7 |
B | SO2和湿润的 | 二者混合后漂白性更强 |
C | 常温下铜与浓硝酸反应可以制取 | 常温下铁与浓硝酸反应也可以制取 |
D | 较强酸可以制取较弱酸 |
|
A.AB.BC.CD.D
【题目】干燥剂的干燥性能可用干燥干燥效率(1立方米空气中实际余留水蒸气的质量![]() 来衡量
来衡量![]() 某些干燥剂的干燥效率如下:
某些干燥剂的干燥效率如下:
物质 | MgO | CaO | ZnCl2 | ZnBr2 |
干燥效率 | 0.008 | 0.2 | 0.8 | 1.1 |
根据以上数据,有关叙述错误的是
A. MgO的干燥性能比CaO差 B. 干燥效率可能与干燥剂的阴阳离子半径大小有关
C. MgCl2可能是比CaCl2更好的干燥剂 D. 上述干燥剂中阳离子对干燥性能的影响比阴离子大