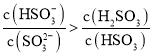��Ŀ����
����Ŀ����һij�о���ѧϰС���ڻ�ѧʵ������ʱ̽��������ԭ����ͭʵ�飮
��1�����ۼ��㣺��ȡ24.0g CuO����ʵ�飬��H2������Ӧ�ÿ��Եõ�Cu������Ϊ______ g
��2��ʵ�飺��24.0g CuO��ȫ��ɺ�ɫ���壬��ȴ���������ù���20.4g���������������ѧ������Ȥ��
��3��һ��ѧ���������ϣ�
��H2��ԭCuOʱ�����ܵõ�������ͭ��CuO����CuOΪ��ɫ���壬������ˮ��
��Cu2O����ϡ���ᷴӦ��CuO+HSO=CuSO+Cu+HO��
��Cu2O����ϡ���ᷴӦ��3CuO+14HNO��ϡ��=6Cu��NO��+2NO��+7HO��
����Cu����ϡ���ᷴӦ��3Cu+8HNO��ϡ��=3Cu��NO��+2NO��+4HO��
���ۣ�����ѡ��������______������ϡ����������ϡ���������жϺ�ɫ�����л���Cu2O�� ������______��
��4����һ��ѧ����Ϊͨ�����㣬����ȷ�Ϲ���ɷ���Cu��Cu2O�Ļ���20.4g��ɫ������Cu2O�����ʵ���Ϊ______mol����20.4g��ɫ������뵽���Ϊ200mL������ϡ�����У�����ԭ����������ʵ���Ϊ______mol��
���𰸡�19.2 ϡ���� ��Һ����ɫͬʱ�к�ɫ������� 0.075 0.15
��������
(1)����ͭԪ���غ����ͭ��������
(3)������Ϣ���֪��Cu2O����ϡ���ᷴӦ����ͭ������ͭ�����ݢ���֪��Cu2O��Cu������ϡ���ᷴӦ��������ͭ��һ��������
(4)��CuΪxmol��Cu2OΪymol������������![]() ���ɴ�ȷ��Cu2O�����ʵ�������ɫ������뵽������ϡ�����У�ͭ����������+2��ͭ���ӣ�������еĵ���+5�۱���ԭΪ+2�۵�NO�����ݵ��ӵ�ʧ�غ���㱻��ԭ����������ʵ�����
���ɴ�ȷ��Cu2O�����ʵ�������ɫ������뵽������ϡ�����У�ͭ����������+2��ͭ���ӣ�������еĵ���+5�۱���ԭΪ+2�۵�NO�����ݵ��ӵ�ʧ�غ���㱻��ԭ����������ʵ�����
(1)24.0g CuO��ͭԪ�ص�����Ϊ![]() g��19.2g������ͭԪ���غ��֪���Եõ�Cu������Ϊ19.2g��
g��19.2g������ͭԪ���غ��֪���Եõ�Cu������Ϊ19.2g��
(3)������Ϣ���֪��Cu2O����ϡ���ᷴӦ����ͭ������ͭ�����ݢ���֪��Cu2O��Cu������ϡ���ᷴӦ��������ͭ��һ���������������������ж��Ƿ���Cu2O������ѡ��ϡ���ᣬ����Һ����ɫͬʱ�к�ɫ������֣���˵����Cu2O��
(4)��CuΪxmol��Cu2OΪymol������������![]() ��x��0.15mol��y��0.075mol������Cu2O�����ʵ���Ϊ0.075mol����ɫ������뵽������ϡ�����У�ͭ����������+2��ͭ���ӣ�����ת�Ƶ����ʵ���Ϊ0.15mol��2+0.075mol��2��0.45mol��������еĵ���+5�۱���ԭΪ+2�۵�NO�����ݵ��ӵ�ʧ�غ��֪����ԭ����������ʵ���Ϊ
��x��0.15mol��y��0.075mol������Cu2O�����ʵ���Ϊ0.075mol����ɫ������뵽������ϡ�����У�ͭ����������+2��ͭ���ӣ�����ת�Ƶ����ʵ���Ϊ0.15mol��2+0.075mol��2��0.45mol��������еĵ���+5�۱���ԭΪ+2�۵�NO�����ݵ��ӵ�ʧ�غ��֪����ԭ����������ʵ���Ϊ![]() ��0.15mol��
��0.15mol��

����Ŀ��CO��SO2����Ҫ�Ĵ�����Ⱦ���壬���û�ѧ��Ӧԭ����������Ⱦ����Ҫ������
I.�״���һ������ȼ�ϣ��״�ȼ�ϵ�ؼ�����ʵ��������ҵ����������ҵ��һ����CO��H2Ϊԭ�Ϻϳɼ״����÷�Ӧ���Ȼ�ѧ����ʽΪ��CO��g��+2H2��g��![]() CH3OH��g�� ��H1��-116kJ��mol-1
CH3OH��g�� ��H1��-116kJ��mol-1
��1�����д�ʩ������������÷�Ӧ�ķ�Ӧ���ʵ���___��
A����ʱ��CH3OH�뷴Ӧ�������� B�����ͷ�Ӧ�¶�
C��������ϵѹǿ D��ʹ�ø�Ч����
��2����֪��CO��g��+2H2��g��![]() CH3OH��g�� ��H1��-116kJ��mol-1
CH3OH��g�� ��H1��-116kJ��mol-1
CO��g��+![]() O2(g)=CO2��g�� ��H2��-283kJ��mol-1
O2(g)=CO2��g�� ��H2��-283kJ��mol-1
H2��g��+![]() O2(g)=H2O(g) ��H3
O2(g)=H2O(g) ��H3
��ѧ�� | H��H | O=O | O��H |
����/KJmol-1 | 436 | 498 | 463.5 |
���H3=___����ʾ1mol��̬�״���ȫȼ������CO2��ˮ����ʱ���Ȼ�ѧ����ʽΪ___��
��.���¶ȸ���500 Kʱ����ѧ�ҳɹ����ö�����̼�������ϳ����Ҵ���2CO2��g����6H2��g��![]() C2H5OH��g����3H2O��g�������ڽ��ܼ��š�����̼�ŷŷ�������ش����塣�ش��������⣺
C2H5OH��g����3H2O��g�������ڽ��ܼ��š�����̼�ŷŷ�������ش����塣�ش��������⣺
��1����ƽ�ⳣ������ʽΪK=____��
��2���ں����ܱ������У��ж�������Ӧ�ﵽƽ��״̬��������___��
a����ϵѹǿ���ٸı� b��H2��Ũ�Ȳ��ٸı�
c��������ܶȲ���ʱ��ı� d����λʱ��������H2��CO2�����ʵ���֮��Ϊ3��1
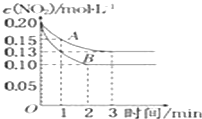
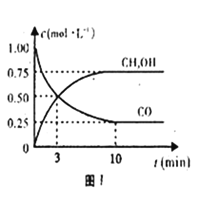
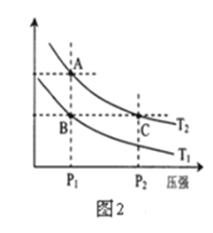
��3����һ��ѹǿ�£������CO2��ȡCH3CH2OH��ʵ�������У���ʼͶ�ϱȡ��¶���CO2��ת���ʵĹ�ϵ��ͼ������ͼ������
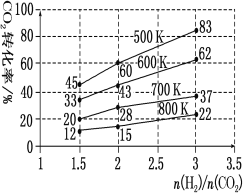
�ٽ����¶ȣ�ƽ����____�����ƶ���
����700K����ʼͶ�ϱ�![]() =1.5ʱ��H2��ת����Ϊ___��
=1.5ʱ��H2��ת����Ϊ___��
����500K����ʼͶ�ϱ�![]() ��2ʱ���ﵽƽ���H2��Ũ��Ϊamol��L��1����ﵽƽ��ʱCH
��2ʱ���ﵽƽ���H2��Ũ��Ϊamol��L��1����ﵽƽ��ʱCH
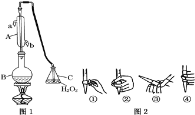
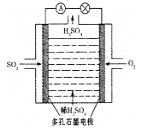
��.ijѧϰС����SO2Ϊԭ�ϣ�����ԭ��ط���ȡ���ᡣ��С����Ƶ�ԭ���ԭ����ͼ��ʾ���õ�����Ҳ�Ϊ___����д���õ�ظ����ĵ缫��Ӧʽ___��
����Ŀ��ͭ��п���仯������;�㷺���ش��������⣺
��1��Zn2+�ļ۲���ӹ������ʽΪ__��
��2��Ԫ�صڶ������ܣ�I2����Zn_Cu���������������������
��3��±��п���۵������ʾ��
ZnF2 | ZnCl2 | ZnBr2 | ZnI2 | |
�ܵ�/�� | 872 | 275 | 394 | 446 |
��ZnCl2��ZnBr2��ZnI2���۵�ʱ��б仯���ɵ�ԭ��___��
��ZnF2���۵�Զ������������±��п����ԭ��Ϊ___��
��4���ڰ�����ण� ����ͭ��������л����Գƺϳ�������յ�ЧӦ����ṹ��ʽ��ͼ��ʾ��
����ͭ��������л����Գƺϳ�������յ�ЧӦ����ṹ��ʽ��ͼ��ʾ��
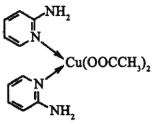
���ڰ�����व�ͭ������У�Cԭ���ӻ�����Ϊ__��
��1mol![]() ����������������Ŀ֮��Ϊ__��
����������������Ŀ֮��Ϊ__��
��5��ͭ�ľ���Ϊ������������ͼ��ʾ������֪��������Ϊa����þ����Ŀռ�������Ϊ__����Բ����Ϊ������