题目内容
5.实验室制备苯乙酮的化学方程式为: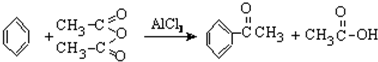 (乙酸酐)制备过程中还有CH3COOH+AlCl3→CH3COOAlCl2+HCl↑等副反应.
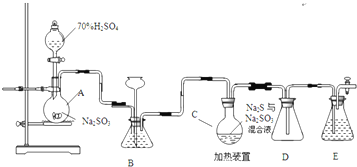
(乙酸酐)制备过程中还有CH3COOH+AlCl3→CH3COOAlCl2+HCl↑等副反应.主要实验装置如图1,步骤如下:
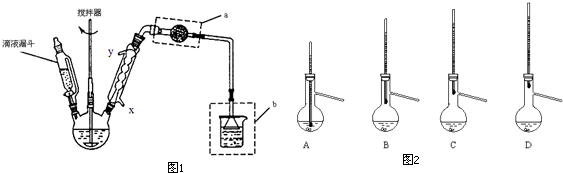
(Ⅰ)合成:在三颈瓶中加入 20g无水AlCl3和30mL无水苯.为避免反应液升温过快,边搅拌边慢慢滴加6mL乙酸酐和10mL无水苯的混合液,控制滴加速率,使反应液缓缓回流.滴加完毕后加热回流1小时.
(Ⅱ)分离与提纯:
①边搅拌边慢慢滴加一定量浓盐酸与冰水混合液,分离得到有机层
②水层用苯萃取,分液
③将①②所得有机层合并,洗涤、干燥、蒸去苯,得到苯乙酮粗产品
④蒸馏粗产品得到苯乙酮.回答下列问题:
(1)球形冷凝管中,冷凝水应从x(填“x”或“y”)口通入;仪器a的作用为:吸水,防止烧杯中的水蒸气进入三角瓶中;装置b的作用:吸收HCl气体.
(2)若将乙酸酐和苯的混合液一次性倒入三颈瓶,可能导致AD.
A.反应太剧烈 B.液体太多搅不动 C.反应变缓慢 D.副产物增多
(3)分离和提纯操作②的目的是把溶解在水中的苯乙酮提取出来以减少损失.该操作中是否可改用乙醇萃取?否(填“是”或“否”),原因是乙醇与水混溶.
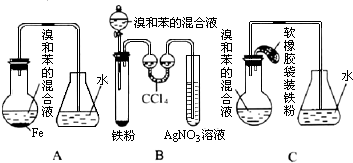
(4)粗产品蒸馏提纯时,图2装置中温度计位置正确的是C,可能会导致收集到的产品中混有低沸点杂质的装置是AB.
分析 (1)根据逆流冷却效果好判断进水口,依据装置图中的仪器和所呈试剂判断仪器的名称和作用;
(2)乙酸酐和苯反应剧烈,温度过高会生成更多的副产物;
(3)依据萃取的原理是利用物质在互不相溶的溶剂中 的溶解度不同,对混合溶液进行分离;
(4)依据蒸馏装置的目的是控制物质的沸点,在一定温度下馏出物质;温度计水银球是测定蒸馏烧瓶支管口处的蒸气温度.
解答 解:(1)根据逆流冷却效果好可知进水口为x,仪器a为干燥管可以吸水,防止烧杯中的水蒸汽进入三角瓶中,装置b的作用是吸收反应过程中所产生的HCl气体;
故答案为:x;防止烧杯中的水蒸汽进入三角瓶中;吸收HCl气体;
(2)若将乙酸酐和苯的混合液一次性倒入三瓶颈,可能会导致反应太剧烈,反应液升温过快导致更多的副产物,
故答案为:AD;
(3)水层用苯萃取并分液的目的是把溶解在水中的苯乙酮提取出来以减少损失,由于乙醇能与水混溶不分层,所以不能用酒精代替苯进行萃取操作;
故答案为:把溶解在水中的苯乙酮提取出来以减少损失;否,乙醇与水混溶;
(4)粗产品蒸馏提纯时,温度计的水银球要放在蒸馏烧瓶支管口处,漏斗装置中的温度计位置正确的是C项,若温度计水银球放在支管口以下位置,会导致收集的产品中 混有低沸点杂质;若温度计水银球放在支管口以上位置,会导致收集的产品中混有高沸点杂质;所以A、B项的装置容易导致低沸点杂质混入收集到的产品中;
故答案为:C;AB.
点评 本题考查了物质制备、分离、提纯、萃取剂选择、仪器使用等试验基础知识的应用,化学实验基本知识和基本技能的掌握是解题关键,题目难度中等.

练习册系列答案
 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
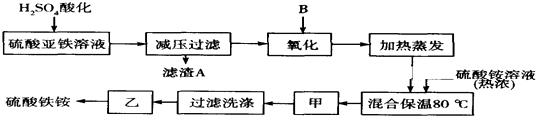
17. 硫酸亚铁铵是一种浅蓝绿色晶体,俗称摩尔盐.
硫酸亚铁铵是一种浅蓝绿色晶体,俗称摩尔盐.
其化学式为:FeSO4•(NH4)2SO4•6H2O 硫酸亚铁在空气中易被氧化,而形成摩尔盐后就稳定了.硫酸亚铁铵可由硫酸亚铁与硫酸铵等物质的量混合制得.三种盐的溶解度(单位为g/100g水)如下表:
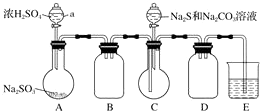
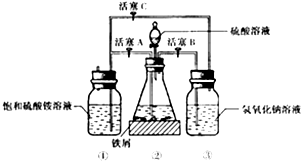
如图是模拟工业制备硫酸亚铁铵晶体的实验装置
回答下列问题:
Ⅰ.(1)先用30%的氢氧化钠溶液煮沸废铁屑(含少量油污、铁锈、FeS等),再用清水洗净,用氢氧化钠溶液煮沸的目的是除去铁屑中油污
(2)将处理好的铁屑放入锥形瓶中,加入稀硫酸,锥形瓶中发生反应的离子方程式可能为ABCD(填序号)
A.Fe+2H+═Fe2++H2↑ B.Fe2O3+6H+═2Fe3++3H2O
C.2Fe3++H2S═2Fe2++S↓+2H+ D.2Fe3++Fe═3Fe2+
(3)利用容器②的反应,向容器①中通入氢气,应关闭活塞A,打开活塞BC(填字母).容器③中NaOH溶液的作用是吸收硫化氢气体,防止污染空气;向容器①中通人氢气的目的是防止亚铁离子被氧气氧化
Ⅱ.待锥形瓶中的铁屑快反应完时,关闭活塞B、C,打开活塞A,继续产生的氢气会将锥形瓶中的硫酸亚铁(含极少部分未反应的稀硫酸)压到饱和硫酸铵溶液的底部.在常温下放置一段时间,试剂瓶底部将结晶出硫酸亚铁铵.硫酸亚铁与硫酸铵溶液混合就能得到硫酸亚铁铵晶体,其原因是硫酸亚铁铵的溶解度最小;从容器①中分离并得到纯净硫酸亚铁铵晶体的操作方法是过滤、用酒精洗涤、干燥
Ⅲ.制得的硫酸亚铁铵晶体中往往含有极少量的Fe3+,为测定晶体中Fe2+的含量,称取一份质量为20.0g的硫酸亚铁铵晶体样品,制成溶液.用0.5mo1/LKMnO4溶液滴定,当溶液中Fe2+全部被氧化,MnO?4被还原成Mn2+时,耗KMnO4溶液体积20.00mL.滴定时,将KMnO4溶液装在酸式(填酸式或碱式)滴定管中,判断反应到达滴定终点的现象为溶液刚出现紫红色,保持30s不变;晶体中FeSO4的质量分数为38%.
 硫酸亚铁铵是一种浅蓝绿色晶体,俗称摩尔盐.
硫酸亚铁铵是一种浅蓝绿色晶体,俗称摩尔盐.其化学式为:FeSO4•(NH4)2SO4•6H2O 硫酸亚铁在空气中易被氧化,而形成摩尔盐后就稳定了.硫酸亚铁铵可由硫酸亚铁与硫酸铵等物质的量混合制得.三种盐的溶解度(单位为g/100g水)如下表:
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 70 |
| (NH4)2SO4 | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 | 91.9 |
| FeSO4•7H2O | 40.0 | 48.0 | 60.0 | 73.3 | - | - |
| 摩尔盐 | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 | 38.5 |
回答下列问题:
Ⅰ.(1)先用30%的氢氧化钠溶液煮沸废铁屑(含少量油污、铁锈、FeS等),再用清水洗净,用氢氧化钠溶液煮沸的目的是除去铁屑中油污
(2)将处理好的铁屑放入锥形瓶中,加入稀硫酸,锥形瓶中发生反应的离子方程式可能为ABCD(填序号)
A.Fe+2H+═Fe2++H2↑ B.Fe2O3+6H+═2Fe3++3H2O
C.2Fe3++H2S═2Fe2++S↓+2H+ D.2Fe3++Fe═3Fe2+
(3)利用容器②的反应,向容器①中通入氢气,应关闭活塞A,打开活塞BC(填字母).容器③中NaOH溶液的作用是吸收硫化氢气体,防止污染空气;向容器①中通人氢气的目的是防止亚铁离子被氧气氧化
Ⅱ.待锥形瓶中的铁屑快反应完时,关闭活塞B、C,打开活塞A,继续产生的氢气会将锥形瓶中的硫酸亚铁(含极少部分未反应的稀硫酸)压到饱和硫酸铵溶液的底部.在常温下放置一段时间,试剂瓶底部将结晶出硫酸亚铁铵.硫酸亚铁与硫酸铵溶液混合就能得到硫酸亚铁铵晶体,其原因是硫酸亚铁铵的溶解度最小;从容器①中分离并得到纯净硫酸亚铁铵晶体的操作方法是过滤、用酒精洗涤、干燥
Ⅲ.制得的硫酸亚铁铵晶体中往往含有极少量的Fe3+,为测定晶体中Fe2+的含量,称取一份质量为20.0g的硫酸亚铁铵晶体样品,制成溶液.用0.5mo1/LKMnO4溶液滴定,当溶液中Fe2+全部被氧化,MnO?4被还原成Mn2+时,耗KMnO4溶液体积20.00mL.滴定时,将KMnO4溶液装在酸式(填酸式或碱式)滴定管中,判断反应到达滴定终点的现象为溶液刚出现紫红色,保持30s不变;晶体中FeSO4的质量分数为38%.
12. 在某密闭容器中,可逆反应:A(g)+B(g)?C(g)符合图中(Ⅰ)所示关系,φ(C)表示C气体在混合气体中的体积分数.由此判断,对图象(Ⅱ)说法不正确的是( )
在某密闭容器中,可逆反应:A(g)+B(g)?C(g)符合图中(Ⅰ)所示关系,φ(C)表示C气体在混合气体中的体积分数.由此判断,对图象(Ⅱ)说法不正确的是( )
 在某密闭容器中,可逆反应:A(g)+B(g)?C(g)符合图中(Ⅰ)所示关系,φ(C)表示C气体在混合气体中的体积分数.由此判断,对图象(Ⅱ)说法不正确的是( )
在某密闭容器中,可逆反应:A(g)+B(g)?C(g)符合图中(Ⅰ)所示关系,φ(C)表示C气体在混合气体中的体积分数.由此判断,对图象(Ⅱ)说法不正确的是( )| A. | p3>p4,Y轴表示A的转化率 | |
| B. | p3>p4,Y轴表示B的质量分数 | |
| C. | p3>p4,Y轴表示B的转化率 | |
| D. | p3>p4,Y轴表示混合气体的平均相对分子质量 |
 .
.