题目内容
14.硫代硫酸钠是一种重要的化工产品.某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3•5H2O).Ⅰ.[查阅资料]
(1)Na2S2O3•5H2O是无色透明晶体,易溶于水,其稀溶液与BaCl2溶液混合无沉淀生成.
(2)向Na2CO3和Na2S混合溶液中通入SO2可制得Na2S2O3,所得产品常含有少量Na2SO3和Na2SO4
(3)Na2SO3易被氧化;BaSO3难溶于水,可溶于稀HCl.
Ⅱ.[制备产品]
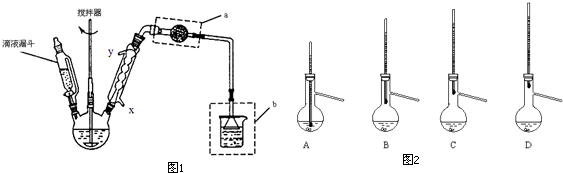
实验装置如图所示(省略夹持装置):
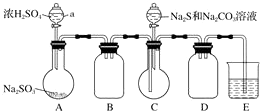
实验步骤:
(1)检查装置气密性,按图示加入试剂.
仪器a的名称是分液漏斗;E中的试剂是B(选填下列字母编号)
A.稀H2SO4
B.NaOH溶液
C.饱和NaHSO3溶液
(2)先向C中烧瓶加入Na2S和Na2CO3混合溶液,再向A中烧瓶滴加浓H2SO4
(3)待Na2S和Na2CO3完全消耗后,结束反应.过滤C中混合物,滤液经蒸发(填写操作名称)、结晶、过滤、洗涤、干燥,得到产品.
Ⅲ.[探究与反思]
(1)为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案,请将方案补充完整.
(所需试剂从稀HNO3、稀H2SO4、稀HCl、蒸馏水中选择)
取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,过滤,用蒸馏水洗涤沉淀,向沉淀中加入足量稀盐酸,若沉淀未完全溶解,并有刺激性气味的气体产生,则可确定产品中含有Na2SO3和Na2SO4.
(2)为减少装置C中生成Na2SO4的量,在不改变原有装置的基础上对实验步骤(2)进行了改进,改进后的操作是先向A中烧瓶滴加浓硫酸,产生的气体将装置中的空气排尽后,再向C中烧瓶加入硫化钠和碳酸钠的混合溶液.
(3)Na2S2O3•5H2O的溶解度随温度升高显著增大,所得产品通过重结晶方法提纯.
分析 Ⅱ.(1)仪器a的名称是分液漏斗;E装置目的是吸收剩余的二氧化硫,因为二氧化硫能与氢氧化钠溶液反应,与稀H2SO4和饱和NaHSO3溶液不反应;
(3)根据将Na2S2O3结晶析出的操作分析;
Ⅲ.【探究与反思】
(1)根据:Na2S2O3•5H2O是无色透明晶体,易溶于水,其稀溶液与BaCl2溶液混合无沉淀生成;Na2SO3易被氧化;BaSO3难溶于水,可溶于稀HCl;BaSO4难溶于水,难溶于稀HCl;硝酸、硫酸、盐酸等性质比较可知;
(2)根据亚硫酸钠易被氧化生成硫酸钠分析;
(3)根据重结晶的适用范围分析.
解答 解:Ⅱ.(1)仪器a的名称是分液漏斗;E中的试剂是NaOH溶液,目的是吸收剩余的二氧化硫,因为二氧化硫能与氢氧化钠溶液反应,与稀H2SO4和饱和NaHSO3溶液不反应,
故答案为:分液漏斗;B;
(3)将Na2S2O3结晶析出的操作应为:蒸发、结晶、过滤、洗涤、干燥,故答案为:蒸发;
Ⅲ.【探究与反思】
(1)根据:Na2S2O3•5H2O是无色透明晶体,易溶于水,其稀溶液与BaCl2溶液混合无沉淀生成;Na2SO3易被氧化;BaSO3难溶于水,可溶于稀HCl;BaSO4难溶于水,难溶于稀HCl,以及硝酸具有强氧化性、加入硫酸会引入硫酸根离子可知,取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,过滤,用蒸馏水洗涤沉淀,向沉淀中加入足量稀盐酸,若沉淀未完全溶解,并有刺激性气味的气体产生,则可以确定产品中含有Na2SO3和Na2SO4,
故答案为:过滤,用蒸馏水洗涤沉淀,向沉淀中加入足量稀盐酸;
(2)因为亚硫酸钠易被氧化生成硫酸钠,所以为减少装置C中生成Na2SO4的量,改进后的操作是先向A中烧瓶滴加浓硫酸,产生的气体将装置中的空气排尽后,再向C中烧瓶加入硫化钠和碳酸钠的混合溶液,
故答案为:先向A中烧瓶滴加浓硫酸,产生的气体将装置中的空气排尽后,再向C中烧瓶加入硫化钠和碳酸钠的混合溶液;
(3)Na2S2O3•5H2O的溶解度随温度升高显著增大,所得产品通过重结晶方法提纯,故答案为:重结晶.
点评 本题以某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3•5H2O)为载体,考查了物质的分离提纯、检验、设计优化等,综合性较强,难度中等.

| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | J | |||||||
| 2 | E | R | F | |||||
| 3 | A | C | D | H | I | G | ||
| 4 | B |
 .
.(2)A、C、D三种元素的氧化物对应的水化物中碱性最强的是NaOH
(3)A、B、C、G的离子按离子半径由大到小的顺序排列为Cl->K+>Na+>Mg2+
(4)写出A的单质与水反应的离子方程式2Na+2H2O=2Na++2OH-+H2↑.
(5)X元素是A~R九种元素中的一种,X的原子核里有14个中子,2.7gX在氧气里燃烧时,质量增加2.4g.X的氢氧化物既能溶于氢氧化钠溶液中反应,也能与盐酸反应.X的元素符号是Al,它位于元素周期表中第三周期、第ⅢA族.
(6)有两种化合物M和N都由AFIJ四种元素组成.若M与N在水溶液中能发生离子反应,则该反应的离子方程式为HSO3-+H+=H2O+SO2↑.
(7)上述元素中最高价氧化物对应的水化物的酸性最强的是HClO4.

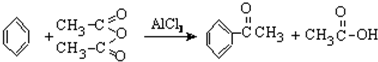 (乙酸酐)制备过程中还有CH3COOH+AlCl3→CH3COOAlCl2+HCl↑等副反应.
(乙酸酐)制备过程中还有CH3COOH+AlCl3→CH3COOAlCl2+HCl↑等副反应.