题目内容
下列溶液中,微粒浓度关系正确的是
A.在0.1mol·L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
B.等体积、等物质的量浓度的NaOH溶液与NaHCO3溶液混合后的溶液:c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
C.0.2mol/L的某一元弱酸HA溶液和0.1mol/LNaOH溶液等体积混合后的溶液:2c(OH-)+c(A-)=2c(H+)+c(HA)
D.常温下,NH4Cl和NH3·H2O的混合溶液[pH=7,c(Cl-)=0.1mol/L]中:c(Cl-)>c(NH4+)>c(OH-)=c(H+)
练习册系列答案
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
13.下列反应中,能说明氯的氧化性比硫强的反应是( )
| A. | CuCl2+H2S═CuS↓+2HCl | B. | 2HCl+Na2S═2NaCl+H2S | ||
| C. | Cl2+H2S═2HCl+S | D. | 3Cl2+6FeSO4═2Fe2(SO4)3+2FeCl3 |


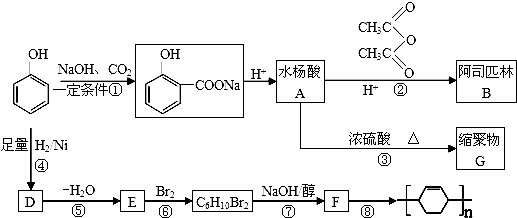
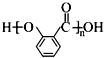 ;⑤的反应条件是NaOH的醇溶液、加热;⑧的反应类型是加聚反应.
;⑤的反应条件是NaOH的醇溶液、加热;⑧的反应类型是加聚反应.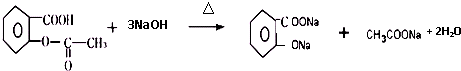 .
.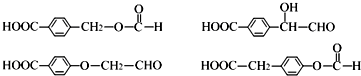 .
.

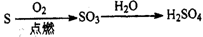
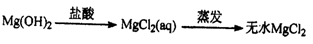



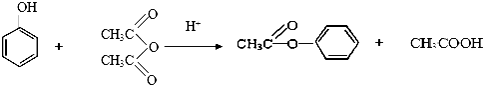
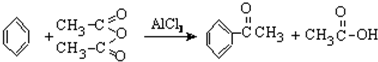 (乙酸酐)制备过程中还有CH3COOH+AlCl3→CH3COOAlCl2+HCl↑等副反应.
(乙酸酐)制备过程中还有CH3COOH+AlCl3→CH3COOAlCl2+HCl↑等副反应.