题目内容
【题目】课题式研究性学习是培养学生创造思维的良好方法。某研究性学习小组将下列装置如图连接,D、E、X、Y都是铂电极、C、F是铁电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答下列问题:

(1)B极的名称是___。
(2)甲装置中电解反应的总化学方程式是:___。
(3)设电解质溶液过量,电解后乙池中加入___(填物质名称)可以使溶液复原。
(4)设甲池中溶液的体积在电解前后都是500ml,乙池中溶液的体积在电解前后都是200mL,当乙池所产生气体的体积为4.48L(标准状况)时,甲池中所生成物质的物质的量浓度为___mol/L;乙池中溶液的pH=___;
(5)装置丁中的现象是___。
【答案】负极 Fe+CuSO4![]() FeSO4+Cu 氯化氢 0.2 14 红褐色由X极移向Y极,最后X附近无色,Y极附近为红褐色
FeSO4+Cu 氯化氢 0.2 14 红褐色由X极移向Y极,最后X附近无色,Y极附近为红褐色
【解析】
(1)电解饱和食盐水时,酚酞变红的极是阴极,串联电路中,阳极连阴极,阴极连阳极,阴极和电源负极相连,阳极和电源正极相连;
(2)根据电解原理来书写电池反应,甲池中C为铁做阳极,D为铂电极,电解质溶液是硫酸铜溶液,依据电解原理分析;
(3)根据电极反应和电子守恒计算溶解和析出金属的物质的量关系;
(4)根据电解反应方程式及气体摩尔体积计算溶液中溶质的物质的量浓度及溶液的pH;
(5)根据异性电荷相吸的原理以及胶体的电泳原理来回答;
(1)向乙中滴入酚酞试液,在F极附近显红色,说明该极上氢离子放电,所以该电极是阴极,所以E电极是阳极,D电极是阴极,C电极是阳极,G电极是阳极,H电极是阴极,X电极是阳极,Y是阴极,A是电源的正极,B是原电池的负极,故答案为:负极;
(2)D、F、X、Y 都是铂电极、C、E是铁电极,甲池中C为铁做阳极,D为铂电极,电解质溶液是硫酸铜溶液,电解硫酸铜溶液时的阳极是铁失电子生成亚铁离子,阴极是铜离子放电,所以电解反应为:Fe+CuSO4![]() FeSO4+Cu,故答案为:Fe+CuSO4
FeSO4+Cu,故答案为:Fe+CuSO4![]() FeSO4+Cu;
FeSO4+Cu;
(3)乙池中电解质过量,F极是铁,作阴极,E为铂作阳极,总反应为:2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑,溶液中放出Cl2和H2,则加入HCl可以使溶液复原,故答案为:氯化氢;
2NaOH+Cl2↑+H2↑,溶液中放出Cl2和H2,则加入HCl可以使溶液复原,故答案为:氯化氢;
(4)根据2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑计算得,n(NaOH)=2n(Cl2)=
2NaOH+Cl2↑+H2↑计算得,n(NaOH)=2n(Cl2)=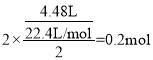 ,则c(H+)=
,则c(H+)=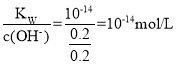 ,则pH=lgc(H+)=lg10-14=14;根据电路中电子转移守恒知:n(FeSO4)=n(Cl2)=0.2mol,则c(FeSO4)=
,则pH=lgc(H+)=lg10-14=14;根据电路中电子转移守恒知:n(FeSO4)=n(Cl2)=0.2mol,则c(FeSO4)= =0.2mol/L,故答案为: 0.2;14;
=0.2mol/L,故答案为: 0.2;14;
(5)根据异性电荷相吸的原理,氢氧化铁胶体中含有的带正电荷的粒子会向阴极即Y极移动,所以Y极附近红褐色变深,故答案为:红褐色由X极移向Y极,最后X附近无色,Y极附近为红褐色。

 名校通行证有效作业系列答案
名校通行证有效作业系列答案【题目】以镍废料(主要成分为镍铁合金,含少量铜)为原料,生产NiO的部分工艺流程如下:
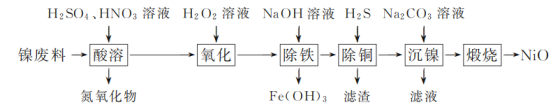
已知:下表列出了几种金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
开始沉淀的pH | 1.5 | 6.5 | 7.7 |
沉淀完全的pH | 3.3 | 9.9 | 9.2 |
(1)“除铁”时需控制溶液的pH范围为________。
(2)“滤渣”的主要成分为________(填化学式)。
(3)“沉镍”时得到碱式碳酸镍[用xNiCO3·yNi(OH)2表示]沉淀。
①在隔绝空气条件下,“煅烧”碱式碳酸镍得到NiO,该反应的化学方程式为________。
②“沉镍”时,溶液pH增大,碱式碳酸镍中Ni元素含量会增加,原因是________。

