题目内容
砷(As)在地壳中含量不大,但砷的化合物却是丰富多彩。
(1)砷的基态原子的电子排布式为 。
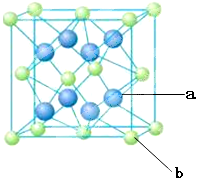
(2)目前市售的发光二极管,其材质以砷化镓(GaAs)为主。Ga和As相比,电负性较大的是 ,GaAs中Ga的化合价为 。
(3)AsH3是无色稍有大蒜气味的气体,在AsH3中As原子的杂化轨道类型为 ;
AsH3的沸点高于PH3,其主要原因为 。
(4)Na3AsO4可作杀虫剂。AsO43-的立体构型为 ,与其互为等电子体的分子的化学式为 (任写一种)。
(5)H3AsO4和H3AsO3是砷的两种含氧酸,请根据结构与性质的关系,解释H3AsO4比H3AsO3酸性强的原因 。
(6)磷与砷同主族,磷的一种单质白磷(P4)属于分子晶体,其晶胞如图。已知最近的两个白磷分子间距离为 a pm,阿伏加德罗常数的值为NA,则该晶体的密度为______g/cm3(只要求列算式,不必计算)。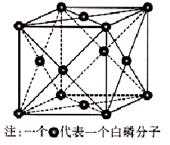
(1)1s22s22p63s23p63d104s24p3 (2分)
(2) As (1分) +3 (1分)
(3)sp3杂化(1分)
AsH3的相对分子质量比PH3的大,分子间作用力大,因而AsH3的沸点比PH3高。(2分,相对分子质量大和分子间作用力大两个给分点各1分。)
(4)正四面体(2分) CF4 SiF4 CCl4 SiCl4等(2分)
(5)H3AsO4和H3AsO3可表示为(HO)3AsO和(HO)3As,H3AsO3中的As为+3价,而H3AsO4中的As为+5价,正电性更高,导致As-O-H中的O的电子更向As偏移,越易电离出H+。(2分)
(6) 或
或  (2分,其他合理答案也可给分)
(2分,其他合理答案也可给分)
解析试题分析:(1)As是33号元素,基态原子核外电子排布为1s22s22p63s23p63d104s24p3。
(2)As、Ga在同一周期,同周期元素电负性自左向右逐渐增大,As在Ga的右面,As的电负性大。As的负化合价为-3,因此Ga的化合价为+3。
(3)AsH3与NH3结构相似,因此AsH3中As的杂化方式为sp3。AsH3、PH3属于分子晶体,相对分子质量越大,熔、沸点越高。
(4)根据ABn型分子构型判断方法,AsO43-的电子对有(5+3)/2=4对,中心原子sp3杂化,因此空间构型为正四面体构型。
5核32电子的分子有CF4 SiF4 CCl4 SiCl4等。
(5)酸性强弱主要看是否容易电离出H+,因此分析出H3AsO4易电离出H+的原因即可。
(6)每一个晶胞中含有的白磷分子数为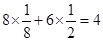 个,晶胞的棱长为
个,晶胞的棱长为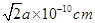 ,每个晶胞的质量为
,每个晶胞的质量为 ,因此晶胞的密度为
,因此晶胞的密度为 。
。
考点:考查原子核外电子排布,电负性,空间构型,晶体性质比较,轨道杂化方式,等电子体,晶胞密度计算等。

 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题: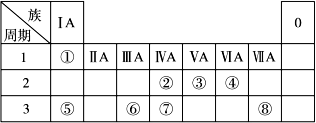
(1)地壳中含量居于第二位的元素在周期表中的位置是________________。
(2)②的最高价氧化物固态时的晶体类型:______________;⑦的最高价氧化物固态时的晶体类型:______________。
(3)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式______________,______________。若用球棍模型表示①和④形成的化合物的分子结构,应该是_____________。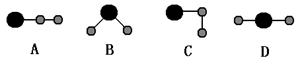
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是( )
| A.最高正化合价为+6价, | B.气态氢化物比H2S稳定, |
| C.最高价氧化物的水化物的酸性比硫酸弱, | D.单质在常温下可与氢气化合。 |
(6)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
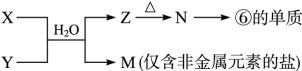
X溶液与Y溶液反应的离子方程式________, M中阳离子的鉴定方法____________。
A、B、C、D是元素周期表前四周期常见的四种元素,原子序数依次增大, 它们的相关结构和性质信息如下表所示,请结合相关信息,完成相关的问题:
| 元素 | 相关结构和性质 |
| A | A为非金属元素,其一种单质是电的良导体,难熔、质软并有润滑性,可用作电极材料 |
| B | 是蛋白质的组成元素之一,原子核外有三种不同能量的电子,且未成对电子数最多 |
| C | 其单质既能与强酸溶液应又能与强碱溶液反应,其简单离子在第三周期单核离子中半径最小 |
| D | D的高价氯化物的盐溶液常用于印刷电路极电路的“刻蚀” |
(1)D位于元素周期表第 周期第 族,其基态原子核外价电子排布式为 ;元素D的高价氯化物形成的盐溶液刻蚀印刷电路板电路所发生反应 的离子方程式为 ;
(2)钠与B元素形成的Na3B晶体属于 晶体(填“分子”、“原子”、“离子”)。 分析B元素的气态氢化物极易溶于水的原因,除了因为它们均是极性分子之外,还因为 ;
(3)元素A与元素B相比,非金属性较强的是 (用元素符号表示),可以作为判断两者非金属性强弱的依据的是 。
a.常温下A的单质和B的单质状态不同
b.该两种原子形成的共价键中共用电子对的偏向
c.最高价氧化物对应水化物的酸性强弱
d.单质与酸反应的难易程度
(4)已知毎5.4g元素C的单质可与元素D的低价氧化物反应,放出346.2kJ的热量。试写出该反应的热化学方程式: 。

 4AC2(g)+B2(g)在上述条件下,向容器中充入AC和BC2各1 mol达平衡时,生成AC2和B2共a mol,则AC的转化率是________(用含a的代数式表示)。
4AC2(g)+B2(g)在上述条件下,向容器中充入AC和BC2各1 mol达平衡时,生成AC2和B2共a mol,则AC的转化率是________(用含a的代数式表示)。