题目内容
1.某化学兴趣小组设计了下图所示实验装置,其中c为石墨电极,d为银电极.
(1)甲池中OH-移向a极(填电极的字母序号),f为阴极(填电极名称).
(2)a极上的电极反应式是CH3OH-6e-+8OH-=CO32-+6H2O.
(3)乙池中放出气体的电极为c极(填“c”或“d”),写出此电极反应式:4OH--4e-═O2↑+2H2O或2H2O-4e-═O2↑+4H+.
(4)乙池中总反应的离子方程式是4Ag++2H2O$\frac{\underline{\;电解\;}}{\;}$4Ag↓+O2↑+4H+.
(5)当乙池中阴极质量增加5.40g时,丙池某电极析出1.60g金属,则丙池的溶液中溶质可能是BD(填序号).
A.MgSO4 B.CuSO4 C.NaCl D.AgNO3.
分析 甲中负极为甲醇,正极为氧气,为原电池,负极反应为CH3OH+8OH-6e-═CO32-+6H2O,乙为电解池,c与原电池的正极相连,则c为阳极,发生4AgNO3+2H2O$\frac{\underline{\;电解\;}}{\;}$4Ag+O2↑+4HNO3,乙中d极析出Ag,阳极极生成氧气,利用电子守恒可知,O2~4Ag~4HNO3,丙池某电极析出1.60g某金属,氧化性比氢离子强的金属离子均可能,以此来解答.
解答 解:(1)燃料电池中,投放燃料的电极是负极,投放氧化剂的电极是正极,原电池放电时,电解质溶液中氢氧根离子向负极移动,即向投放甲醇的电极移动,f连接原电池的负极,则为电解池的阴极,
故答案为:a;阴极;
(2)该燃料电池中,甲醇失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为:CH3OH-6e-+8OH-=CO32-+6H2O,
故答案为:CH3OH-6e-+8OH-=CO32-+6H2O;
(3)乙池有外接电源属于电解池,连接原电池正极的c是阳极,连接原电池负极的B是阴极,电解硝酸银溶液时,c电极上氢氧根离子放电,电极反应式为4OH--4e-=O2↑+2H2O或2H2O-4e-═O2↑+4H+,
故答案为:c;4OH--4e-═O2↑+2H2O或2H2O-4e-═O2↑+4H+;
(4)乙池为电解硝酸银的反应,总反应的离子方程式是4Ag++2H2O$\frac{\underline{\;电解\;}}{\;}$4Ag↓+O2↑+4H+,
故答案为:4Ag++2H2O$\frac{\underline{\;电解\;}}{\;}$4Ag↓+O2↑+4H+;
(5)A.硫酸镁中镁元素处于H元素前,所以阴极上不析出金属单质,故错误;
B.电解硫酸铜溶液时,阴极上析出1.60g铜需要转移电子0.05mol,故正确;
C.氯化钠中钠元素处于氢元素前,所以阴极上不析出金属单质,故错误;
D.电解硝酸银溶液时,阴极上析出1.60g银需要转移电子0.0148mol<0.05mol,故正确;
故答案为:BD.
点评 本题考查原电池和电解池,明确发生的电极反应、离子的放电顺序即可解答,注意电子守恒在计算中的应用,题目难度中等,注重了基础知识的考查.

| A. | LiH、LiD、LiT的摩尔质量之比为1:2:3 | |
| B. | 一个T原子的质量约为$\frac{2}{6.02}$×1023g | |
| C. | H、D、T的中子数之比为1:2:3 | |
| D. | 氕化锂、氘化锂、氚化锂都是强还原剂 |
| A. | 铁和盐酸:Fe+2H+═Fe3++H2↑ | |
| B. | 石灰石和硝酸:CO32-+2H+═H2O+CO2↑ | |
| C. | 铜和硝酸银溶液:Cu+Ag+═Cu2++Ag | |
| D. | 氢氧化钡溶液和硫酸:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O |

有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(1)在装置c中应加入③(选填序号),其目的是吸收反应中可能生成的酸性气体.
①水 ②浓硫酸 ③氢氧化钠溶液 ④饱和碳酸氢钠溶液
(2)判断d管中制备二溴乙烷反应已结束的最简单方法是溴的颜色完全褪去.
(3)将二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在水的(填“上”或“下”)下层.
(4)若产物中有少量未反应的Br2,最好用②(填正确选项前的序号)洗涤除去.
①水 ②氢氧化钠溶液 ③碘化钠溶液 ④乙醇
(5)反应过程中需用冷水冷却(装置e),其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但不用冰水进行过度冷却,原因是:1,2-二溴乙烷的凝固点较低,过度冷却会使其凝固而使气路堵塞
(6)以1,2-二溴乙烷为原料,制备聚氯乙烯,为了提高原料利用率,有同学设计了如下流程:1,2-二溴乙烷通过( ①)反应制得( ②),②通过( ③)反应制得氯乙烯,由氯乙烯制得聚氯乙烯.
①消去反应(填反应类型) ②
 (填该物质的电子式)③加成反应(填反应类型)写出第一步的化学方程式
(填该物质的电子式)③加成反应(填反应类型)写出第一步的化学方程式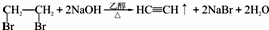 .
. 
 .
.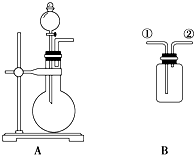 如图A是实验室制取某些气体的装置.
如图A是实验室制取某些气体的装置. 一定条件下,物质A~E转化关系如图,其中A为单质,常温下E为无色液体.
一定条件下,物质A~E转化关系如图,其中A为单质,常温下E为无色液体.