题目内容
【题目】某温度下,向![]() 恒容密闭容器中充入
恒容密闭容器中充入![]() 和
和![]() ,发生反应
,发生反应![]() ,经过一段时间后反应达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是
,经过一段时间后反应达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是![]()
![]()
| 0 | 5 | 15 | 25 | 35 |
|
|
|
|
|
|
A.前![]() 的平均反应速率
的平均反应速率![]()
B.保持其他条件不变,升高温度,平衡时![]() ,则反应的
,则反应的![]()
C.相同温度下,起始时向容器中充入![]() ,达到平衡时C的转化率大于
,达到平衡时C的转化率大于![]()
D.相同温度下,起始时向容器中充入![]() 、
、![]() 和
和![]() ,反应达到平衡前
,反应达到平衡前![]() 正
正![]() 逆
逆![]()
【答案】D
【解析】
A的物质的量为![]() 时反应达到平衡状态,则
时反应达到平衡状态,则
![]()
起始量![]()
![]() 0
0
转化量![]()
![]()
![]()
![]()
平衡量![]()
![]()
![]()
容器容积为![]() ,代入平衡浓度求得平衡常数
,代入平衡浓度求得平衡常数![]() ;
;
A.前![]() 的平均反应速率
的平均反应速率![]() ,故A错误;
,故A错误;
B.保持其他条件不变,升高温度,平衡时![]() ,此时A的物质的量为
,此时A的物质的量为![]() ,说明升温平衡逆向移动,正反应是放热反应,
,说明升温平衡逆向移动,正反应是放热反应,![]() ,故B错误;
,故B错误;
C.起始时加入![]() ,等效于起始时加入
,等效于起始时加入![]() 和
和![]() ,与原平衡相比,压强增大,平衡向正反应方向移动,平衡时A、B的转化率较原平衡高,故平衡时A、B的物质的量均小于
,与原平衡相比,压强增大,平衡向正反应方向移动,平衡时A、B的转化率较原平衡高,故平衡时A、B的物质的量均小于![]() ,C的物质的量大于
,C的物质的量大于![]() ,参加反应的C的物质的量小于
,参加反应的C的物质的量小于![]() ,转化率小于
,转化率小于![]() ,故C错误;
,故C错误;
D.相同温度下,起始时向容器中充入![]() 、
、![]() 和
和![]() ,
,![]() ,反应逆向进行,达到平衡前
,反应逆向进行,达到平衡前![]() 正
正![]() 逆
逆![]() ,故D正确;
,故D正确;
故答案选D。

 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
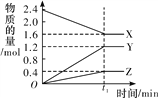
激活思维智能训练课时导学练系列答案【题目】一定温度下,在4个容积均为1 L的恒容容器中分别进行反应(各容器中A都足量)A(s)+B(g)![]() C(g)+D(g) ΔH =+100 kJ·mol-1,某时刻测得部分数据如下表:
C(g)+D(g) ΔH =+100 kJ·mol-1,某时刻测得部分数据如下表:
容器编号 | n(B)/mol | n(C)/mol | n(D)/mol | 反应时间/min | 反应速率 |
Ⅰ | 0.06 | 0.60 | 0.10 | t1 | v(正)=v(逆) |
Ⅱ | 0.12 | 1.20 | 0.20 | t2 | |
Ⅲ | 0.32 | 1.0 | 0 | 0 | |
Ⅳ | 0.12 | 0.30 | v(正)=v(逆) |
下列说法正确的是
A.容器Ⅰ中平均反应速率v(B)=0.04/t1 mol·L-1·min-1
B.t2时容器Ⅱ中v(正)>v(逆)
C.容器Ⅲ
D.容器Ⅳ中c(D)= 0.4 mol·L-1
【题目】有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下:
实验装置 | 部分实验现象 |
| a极质量减小,b极质量增加 |
| b极有气体产生,c极无变化 |
| d极溶解,c极有气体产生 |
| 电流计指示在导线中电流从a极流向d极 |
由此可判断这四种金属的活动性顺序是( )
A.a>b>c>dB.b>c>d>aC.d>a>b>cD.a>b>d>c