题目内容
【题目】聚合硫酸铁[Fe(OH)SO4]n能用做净水剂(絮凝剂),可由绿矾(FeSO47H2O)和KClO3在水溶液中反应得到。下列说法不正确的是( )
A.KClO3作氧化剂,每生成1mol[Fe(OH)SO4]n消耗![]() molKClO3
molKClO3
B.生成聚合硫酸铁后,水溶液的pH增大
C.聚合硫酸铁可在水溶液中水解生成氢氧化铁胶体而净水
D.在反应中氧化剂和还原剂物质的量之比为1:6
【答案】A
【解析】
KClO3将FeSO4氧化成[Fe(OH)SO4]n的化学方程式为6nFeSO4+nKClO3+3nH2O=6[Fe(OH)SO4]n+nKCl,聚合硫酸铁[Fe(OH)SO4]n又称为碱式硫酸铁,能水解生成氢氧化铁胶体,据此解答。
A.KClO3作氧化剂,氧化FeSO4生成[Fe(OH)SO4]n的化学方程式为6nFeSO4+nKClO3+3nH2O=6[Fe(OH)SO4]n+nKCl,所以每生成1mol[Fe(OH)SO4]n消耗![]() mol KClO3,A错误;
mol KClO3,A错误;
B.FeSO4是强酸弱碱盐,水溶液显酸性,聚合硫酸铁又称为碱式硫酸铁,生成聚合硫酸铁后,水溶液的酸性减弱,pH增大,B正确;
C.聚合硫酸铁中的铁为+3 价,其中的Fe3+能水解生成氢氧化铁胶体,氢氧化铁胶体能吸附水中的悬浮物,从而具有净水作用,C正确;
D.在该反应中KClO3作氧化剂,FeSO4作还原剂,根据反应方程式可知氧化剂与还原剂的物质的量的比是1:6,D正确;
故合理选项是A。

 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案【题目】按要求答题
(1)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25℃、101kPa下,已知该反应每消耗1molCuCl(s),放热44.4kJ,该反应的热化学方程式是________
(2)已知E1=134kJ·mol-1、E2=368kJ·mol-1,请参考题中图表,按要求填空:
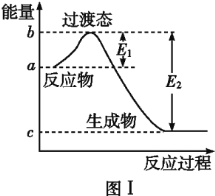
①图Ⅰ是1molNO2(g)和1molCO(g)反应生成CO2(g)和NO(g)过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率加快,E1的变化是________(填“增大”“减小”或“不变”,下同),ΔH的变化是________。NO2和CO反应的热化学方程式为________。
②下表所示是部分化学键的键能参数:
化学键 | P—P | P—O |
|
|
键能/(kJ·mol-1) | a | b | C | x |
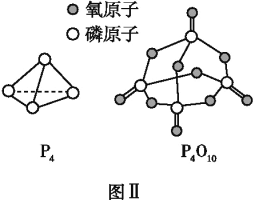
已知P4(g)+5O2(g)P4O10(g)ΔH=-dkJ·mol-1,P4及P4O10的结构如图Ⅱ所示。表中x=________(用含a、b、c、d的代数式表示)。
(3)肼(N2H4)是一种可燃性的液体,可用作火箭燃料。燃烧时释放大量的热并快速产生大量气体。已知在101kPa、298K时,1mol液态N2H4在O2中完全燃烧生成N2和水蒸气,放出热量624kJ,该反应的热化学方程式是________。
又知:H2O(g)=H2O(l)ΔH=-44kJ·mol-1,若1mol液态N2H4在O2中完全燃烧生成N2和液态水,则放出的热量为________kJ。