��Ŀ����
����Ŀ�����ӹ�ҵ����30%��FeCl3��Һ��ʴ���ھ�Ե���ϵ�ͭ��������ӡˢ��·�塣
(1)д��FeCl3��Һ�����ͭ������Ӧ�Ļ�ѧ����ʽ:______________________��
(2)ij����ʦΪ�˴�ʹ�ù��ĸ�ʴ��Һ����Ҫ��CuCl2��FeCl3��Һ�ȣ��л���ͭ�������»�ô�����FeCl3��Һ����������ͼ��ʾ����:����֪���ӹ�����ΪFe���ӹ�����Ϊϡ���ͨ����ΪCl2��
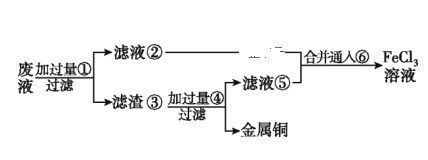
������ʵ��������������Ҫ����Ϊ___________________���ѧʽ����д�����ڢ��ĺϲ�Һ��ͨ���������ӷ���ʽ:______________________________��
�����Ʋ�����FeCl2��Һʱ���������м����Ŀ����_______________________________��
��Ҫ֤��FeCl3��Һ�Ƿ���Fe2+����ѡ������ѡ���е�______________����֪����������ʺ�������ɫ��������
A������ K3[Fe(CN)6]��Һ ��B������NaOH��Һ C������KSCN��Һ
(3)����1.2 L��3 mol FeCl2��������Һǡ����0.6 mol HIO3��ȫ��Ӧ����ԭ����Ϊ_______���ѧʽ����֪��������������Һ���������÷�Ӧ���ӷ���ʽΪ___________________________________��
���𰸡�Cu��2Fe3����Cu2����2Fe2�� Cu��Fe Cl2��2Fe2����2Fe3����2Cl�� ��ֹFe2����������2Fe3����Fe��3Fe2�� A I2 12H+��10Fe2����2IO3����10Fe3����I2��6H2O�� 10H+��10Fe2����2HIO3��10Fe3����I2��6H2O
��������
(1) ͭ���Ȼ�����Ӧ�����Ȼ�ͭ���Ȼ�������
(2) ��Ӧ�к����Ȼ��������Ȼ�ͭ���ɹ������̿�֪���������к��н���ͭ����Ӧ�Ƿ�Һ�������Fe��Ӧ����Һ���к����Ȼ�������ͨ���������Եõ��Ȼ������������к��н���ͭ��δ��Ӧ�������������ᣬ���ˣ�����ͭ����Һ���к����Ȼ�����������Һ�ںϲ����Ʊ��Ȼ������ݴ˽��н��
(3) ��I2����Һ��������Һ��������1.2 L��3 mol FeCl2����Һǡ����0.6 mol HIO3��ȫ��Ӧ����I2��ͬʱ��������������ΪFe3+����������غ㣬��Ӧ��ˮ���ɣ��ݴ�д��������Ӧ�����ӷ���ʽ��
(1) ͭ���Ȼ�����Ӧ�����Ȼ������Ȼ���������Ӧ����ʽΪ��2FeCl3+Cu�T2 FeCl2+CuCl2��
(2) �ɹ������̿�֪���������к��н���ͭ��Ŀ������ȡ�Ȼ�������ҺӦ������������Fe��Ӧ���ʢ�Fe����Һ���к���FeCl2��ͨ����������Եõ��Ȼ������������к��н���Cu��δ��Ӧ��Fe����������ᣬ���ˣ�����ͭ����Һ���к���FeCl2������Һ�ںϲ����Ʊ��Ȼ�����������������֪����Fe ��FeCl2��Fe��Cu ��HCl ��FeCl2��Cl2��
��ʵ�����������к��н���Cu��δ��Ӧ��Fe����ڢݵĺϲ�Һ��ͨ��ķ�Ӧ���������������������������ӣ���Ӧ�����ӷ���ʽΪ��2Fe2++Cl2=2Fe3++2Cl-��
��Fe2+���ӱ�������Ϊ�������е�����������Ϊ�� Fe3+�����Դ�ʱ�������ۣ�����Ϊ���ܽ����ɵ�Fe3+��ԭΪFe2+�����������ӷ�ӦΪ2Fe3++Fe�T3Fe2+��
���ں���Fe2+����Һ�еμ�K3[Fe(CN)6]��Һ������ɫ�������ɣ������Fe2+Ӧѡ��K3[Fe(CN)6]��Һ���ʴ�ΪA��
(3) ��I2����Һ��������Һ��������1.2 L��3 mol FeCl2����Һǡ����0.6 mol HIO3��ȫ��Ӧ����I2��ͬʱ��������������ΪFe3+����������غ㣬��Ӧ��ˮ���ɣ��ݴ�д��������Ӧ�����ӷ���ʽΪ12H+��10Fe2����2IO3����10Fe3����I2��6H2O��