题目内容
【题目】下列离子方程式书写正确的是
A. 醋酸溶解水垢中的CaCO3: CaCO3 + 2H+= Ca2++ H2O + CO2↑
B. 惰性电极电解饱和MgCl2溶液: Mg2++2Cl- + 2H2O ![]() Mg(OH)2↓ + H2↑ + Cl2↑
Mg(OH)2↓ + H2↑ + Cl2↑
C. 苯酚钠溶液中通入少量的CO2:![]() +H2O+CO2→
+H2O+CO2→ +
+![]()
D. 用银氨溶液检验乙醛中的醛基:CH3CHO+![]() +2OH-
+2OH-![]() CH3COONH4+H2O+2Ag↓+3NH3↑
CH3COONH4+H2O+2Ag↓+3NH3↑
【答案】B
【解析】
A.醋酸溶解水垢中的CaCO3的离子方程式为:CaCO3+2CH3COOH= Ca2++ 2CH3COO-+H2O+CO2↑,故A错误;
B.惰性电极电解饱和MgCl2溶液的离子方程式为:Mg2++2Cl- + 2H2O ![]() Mg(OH)2↓+ H2↑+Cl2↑,故B正确;
Mg(OH)2↓+ H2↑+Cl2↑,故B正确;
C.苯酚钠溶液中通入少量的CO2的离子方程式为: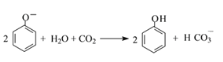 ,故C错误;
,故C错误;
D.用银氨溶液检验乙醛中的醛基:CH3CHO+2Ag(NH3)![]() +2OH-
+2OH-![]() CH3COO-
CH3COO-![]() NH4++H2O+2Ag↓+3NH3,故D错误;
NH4++H2O+2Ag↓+3NH3,故D错误;
本题答案为B。

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是

选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |