题目内容
【题目】Ⅰ.碘酸钾(KIO3)是一种白色或无色固体,可溶于水,具有较强的氧化性。常添加于食盐中用以防治碘缺乏病。已知在某反应体系中存在以下几个物质: KIO3、K2SO4、KI、I2、H2SO4、H2O。
(1)书写并配平该反应方程式,并标出电子转移的方向和数目:_________________;
(2)下列说法中正确的是_________。
A.I2是非电解质 B.K2SO4溶液的导电能力一定比KI溶液的强
C.H2SO4没有参加氧化还原反应 D.氧化产物和还原产物都是I2
Ⅱ.二氧化氯(ClO2)是高效安全的饮用水消毒剂,得到越来越广泛的应用,实验室可用KClO3通过以下反应制得:2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O
试回答下列问题。
(3)该反应中还原产物的化学式是_________;被氧化的元素是_________。
(4)生成标况下4.48LCO2,电子转移数是_______________。
(5)ClO2和Cl2均能将电镀废水中的CN 反应为无毒的物质,自身反应后均生成Cl,此过程说明ClO2和Cl2均具有_________ (填“氧化”或“还原”)性。处理含相同量CN的电镀废水,所需Cl2的物质的量是ClO2的_________倍。
【答案】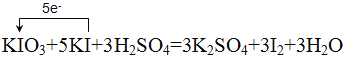 CD ClO2 C 0.2NA 氧化 2.5
CD ClO2 C 0.2NA 氧化 2.5
【解析】
(1)KIO3具有较强的氧化性,KI具有还原性,二者在酸性条件下发生氧化还原反应,生成单质碘;
(2)A.单质既不是电解质,也不是非电解质;B.溶液的导电性与离子浓度有关;C.根据硫酸中是否有元素的化合价发生变化判断;D.根据元素的化合价判断;
(3)2KClO3+H2C2O4+H2SO4═K2SO4+2ClO2↑+2H2O+2CO2↑,反应中,KClO3中Cl元素的化合价由+5价降低为+4价,H2C2O4中C元素的化合价升高,据此分析解答(3)和(4);
(5)Cl2和ClO2被还原后均生成氯离子,根据转移的电子数相等分析计算。
Ⅰ.(1)KIO3具有较强的氧化性,KI具有还原性,二者在酸性条件下发生氧化还原反应,生成单质碘,反应的方程式为:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O;反应中KIO3中I元素由+5价降低为0价,KI中I元素由-1价升高为0价,转移5个电子,电子转移的方向和数目用单线桥表示为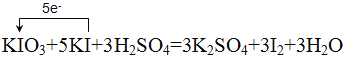 ,故答案为:
,故答案为: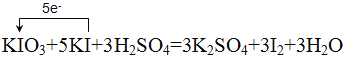 ;
;
(2)A.单质既不是电解质,也不是非电解质,所以I2不是非电解质,故A错误;B.溶液的浓度不知道,无法判断K2SO4溶液与KI溶液的导电性强弱,故B错误;C.反应中生成了硫酸盐,H2SO4中元素的化合价均没有变化,没有参加氧化还原反应,故C正确;D.KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O;反应中KIO3中I元素由+5价降低为0价,KI中I元素由-1价升高为0价,反应中只有I元素的化合价发生了变化,氧化产物和还原产物都是I2,故D正确;故答案为:CD;
Ⅱ.(3)反应中,KClO3中Cl元素的化合价由+5价降低为+4价,被还原,则ClO2是还原产物,H2C2O4中C元素的化合价升高,则C元素被氧化,故答案为:ClO2;C;
(4)2KClO3+H2C2O4+H2SO4═K2SO4+2ClO2↑+2H2O+2CO2↑,KClO3中Cl元素的化合价由+5价降低为+4价,反应中转移电子数为2,即生成2mol CO2转移2mol电子;标况下4.48LCO2的物质的量为![]() =0.2mol,则电子转移数为0.2NA,故答案为:0.2NA;
=0.2mol,则电子转移数为0.2NA,故答案为:0.2NA;
(5)ClO2和Cl2均容易得电子,具有氧化性;有每摩尔Cl2反应生成氯离子得到2mol电子,而每摩尔ClO2反应生成氯离子得到5mol电子,则处理含相同量CN的电镀废水,所需Cl2的物质的量是ClO2的![]() =2.5倍,故答案为:氧化;2.5。
=2.5倍,故答案为:氧化;2.5。

 阅读快车系列答案
阅读快车系列答案