题目内容
苯与乙烯相比较,下列叙述不正确的是( )
| A、都容易发生取代反应 |
| B、苯不能被KMnO4氧化 |
| C、苯只能在特殊条件下发生加成反应 |
| D、都能在空气中燃烧 |
考点:苯的性质,乙烯的化学性质
专题:有机反应
分析:依据乙烯和苯的结构特点:乙烯中含有碳碳双键,苯中不含碳碳双键,苯中的化学键是介于双键和单键之间一种独特的化学键,解答此题.
解答:
解:A.乙烯中含有碳碳双键,易发生加成反应,故A错误;
B.苯中不含碳碳双键,不能被KMnO4氧化,故B正确;
C.苯在催化剂条件下,能够与氢气发生加成反应,生成环己烷,故C正确;
D.苯含碳和氢两种元素,能在空气中燃烧生成二氧化碳和水,故D正确;
故选:A.
B.苯中不含碳碳双键,不能被KMnO4氧化,故B正确;
C.苯在催化剂条件下,能够与氢气发生加成反应,生成环己烷,故C正确;
D.苯含碳和氢两种元素,能在空气中燃烧生成二氧化碳和水,故D正确;
故选:A.
点评:本题考查了苯和乙烯的结构和性质,题目难度不大,明确苯中碳碳键的特殊性是解题关键.

练习册系列答案
相关题目
下列有关说法正确的是( )
| A、同种元素的原子均有相同的质子数和中子数 |
| B、IA族金属元素是同周期中金属性最强的元素 |
| C、ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强 |
| D、2SO2(g)+O2(g)═2SO3(g)和4SO2(g)+2O2(g)═4SO3(g)的△H相等 |
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、0.1mol Fe在过量的Cl2中充分燃烧,转移的电子数为0.3NA |
| B、常温下,22.4L甲烷中含有的共价键数目为4NA |
| C、2mol SO2和1mol O2在密闭容器中催化加热,充分反应后,容器内分子总数为2NA |
| D、由CO2和O2组成的混合气体中共有NA个分子,其中的氧原子数为2NA |
下列叙述正确的是( )
| A、加入铝粉能产生H2的溶液中可能大量共存的离子组:NH4+、Fe2+、SO42-、NO3- |
| B、碳酸氢钠溶液中离子浓度的大小关系c(Na+)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-) |
| C、碳酸钠溶液中离子浓度的关系2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| D、向Ca(ClO)2溶液中通入少量CO2的离子方程式:2ClO-+CO2+H2O═2HClO+CO32- |
下列说法正确的是( )
| A、NaHSO3和NaHCO3的混合溶液中(S和C均用R表示):c(Na+)+c(H+)=c(HRO3-)+c(RO32-)+c(OH-) |
| B、常温下物质的量浓度相等的①(NH4)2CO3、②(NH4)2SO4、③(NH4)2Fe(SO4)2,三种溶液中水的电离程度:③>①>② |
| C、39g Na2O2与足量水反应后转移的电子数为NA(NA表示阿伏加德罗常数的值) |
| D、当6.9g Fe3O4与足量稀HNO3反应(还原产物只有NO),则参加反应的HNO3为0.28mol |
下列微粒在溶液中能大量共存,通入SO2后仍能大量共存的一组是( )
| A、Ba2+、Na+、H+、Cl- |
| B、Na+、K+、SO32-、Cl- |
| C、Al3+、K+、Br-、HCO3- |
| D、Fe3+、Na+、H2O2、SO42- |
常温下,在0.005mol/L H2SO4中,水的离子积是( )
| A、1×10-14 |
| B、1×10-12 |
| C、1×10-24 |
| D、1×10-4 |
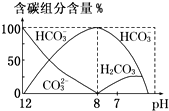 在含有弱电解质的溶液中,往往有多个化学平衡共存.
在含有弱电解质的溶液中,往往有多个化学平衡共存.