题目内容
下列有关说法正确的是( )
| A、同种元素的原子均有相同的质子数和中子数 |
| B、IA族金属元素是同周期中金属性最强的元素 |
| C、ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强 |
| D、2SO2(g)+O2(g)═2SO3(g)和4SO2(g)+2O2(g)═4SO3(g)的△H相等 |
考点:元素周期表的结构及其应用,质量数与质子数、中子数之间的相互关系,反应热和焓变
专题:元素周期律与元素周期表专题
分析:A.同种元素的原子均有相同的质子数,而中子数不同;
B.同周期中从左向右金属性减弱;
C.ⅦA族元素的阴离子还原性越强,对应非金属性越弱;
D.△H与热化学反应中的化学计量数有关.
B.同周期中从左向右金属性减弱;
C.ⅦA族元素的阴离子还原性越强,对应非金属性越弱;
D.△H与热化学反应中的化学计量数有关.
解答:
解:A.同种元素的原子均有相同的质子数,而中子数不同,如H、D、T,故A错误;
B.同周期中从左向右金属性减弱,则IA族金属元素是同周期中金属性最强的元素,故B正确;
C.ⅦA族元素的阴离子还原性越强,对应非金属性越弱,则最高价氧化物对应水化物的酸性越弱,故C错误;
D.△H与热化学反应中的化学计量数成正比,则2SO2(g)+O2(g)═2SO3(g)和4SO2(g)+2O2(g)═4SO3(g)的△H不等,故D错误;
故选B.
B.同周期中从左向右金属性减弱,则IA族金属元素是同周期中金属性最强的元素,故B正确;
C.ⅦA族元素的阴离子还原性越强,对应非金属性越弱,则最高价氧化物对应水化物的酸性越弱,故C错误;
D.△H与热化学反应中的化学计量数成正比,则2SO2(g)+O2(g)═2SO3(g)和4SO2(g)+2O2(g)═4SO3(g)的△H不等,故D错误;
故选B.
点评:本题考查较综合,涉及元素周期表的结构及应用、元素性质变化规律及反应热,为高频考点,注重高频考点的考查,选项D为解答的易错点,题目难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、食品保鲜膜成分为聚氯乙烯 |
| B、甲醛可作为海产品的防腐剂 |
| C、盐析可提纯蛋白质并保持其生理活性 |
| D、医疗上用于消毒的酒精其体积分数为95% |
下列物质中既含有离子键又含有共价键的化合物是( )
| A、NaCl |
| B、CH4 |
| C、KOH |
| D、CH3Cl |
下列叙述正确的是(设NA为阿伏加德罗常数的数值)( )
| A、检验溶液中是否含有Fe2+的方法是先滴加氯水,再滴加KSCN溶液 |
| B、铅蓄电池放电时的负极反应式为:Pb02+4H2SO4+2e-═PbSO4+2H2O |
| C、Na2CO3溶液加水稀释后,恢复至原温度,溶液的pH和Kw均减小 |
| D、某电池的总反应为:5MnO2+2Ag+2NaCl═Na2Mn5O10+2AgCl,每生成1mol Na2Mn5O10转移电子数2NA |
能证明乙烯里含有一个碳碳双键的事实是( )
| A、乙烯能使酸性KMnO4溶液褪色 |
| B、乙烯分子里碳、氢原子个数比为1:2 |
| C、乙烯完全燃烧生成的CO2和H2O的物质的量相等 |
| D、乙烯容易与溴水发生反应,且1 mol乙烯完全加成消耗1 mol溴单质 |
下列各组物质中,可用分液漏斗分离的一组是( )
| A、酒精和水 | B、苯和水 |
| C、乙酸和乙酸乙酯 | D、碘酒和水 |
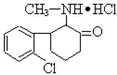 “K”粉医学上称氯胺酮,属于静脉全麻药品,具有一定的精神依赖性.因其物理形状通常为白色粉末,故称“K”粉.目前,该药物已被我国药检部门列为第二类精 神药品管理.其结构简式如下.
“K”粉医学上称氯胺酮,属于静脉全麻药品,具有一定的精神依赖性.因其物理形状通常为白色粉末,故称“K”粉.目前,该药物已被我国药检部门列为第二类精 神药品管理.其结构简式如下.下列说法正确的是( )
| A、“K”粉的化学式为C13H10NOCl2 |
| B、1mol“K”粉在一定条件下可与4mol H2发生加成反应 |
| C、“K”粉分子中至少有7个C原子处于同一平面 |
| D、“K”粉不能与NaOH溶液发生反应 |
推理是研究和学习化学的一种重要方法.以下推理正确的是( )
| A、酸碱发生中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 |
| B、碱中都含有氢氧根,所以碱中一定含有氢元素 |
| C、酸能使紫色石蕊溶液变红,CO2通入紫色石蕊溶液后溶液变红,所以CO2是酸 |
| D、有机物都含碳元素,所以含碳元素的化合物都是有机物 |
苯与乙烯相比较,下列叙述不正确的是( )
| A、都容易发生取代反应 |
| B、苯不能被KMnO4氧化 |
| C、苯只能在特殊条件下发生加成反应 |
| D、都能在空气中燃烧 |