题目内容
17.某化合物受热可完全分解,其中一种气体可使润湿的红色石蕊试纸变蓝,另一气体可澄清石灰水变浑浊.取该化合物溶于水,加入CaCl2溶液,无现象.则该化合物可能是( )| A. | NH4HCO3 | B. | NH4Cl | C. | NH4NO3 | D. | (NH4)2CO3 |
分析 某化合物受热可完全分解,其中一种气体可使润湿的红色石蕊试纸变蓝,说明生成的气体为氨气,原化合物中含有铵根离子,另一气体可澄清石灰水变浑浊,说明生成的气体为二氧化碳或二氧化硫,取该化合物溶于水,加入CaCl2溶液,无现象说明酸根阴离子为酸式酸根离子;
解答 解:某化合物受热可完全分解,其中一种气体可使润湿的红色石蕊试纸变蓝,说明生成的气体为氨气,证明原化合物中含有铵根离子,另一气体可澄清石灰水变浑浊,说明生成的气体为二氧化碳或二氧化硫,取该化合物溶于水,加入CaCl2溶液,无现象说明酸根阴离子为酸式酸根离子,证明含有HCO3-或HSO3-离子,分析选项可知为NH4HCO3,
故选A.
点评 本题考查了物质性质和离子性质的分析判断,主要是铵根离子和碳酸氢根离子特征性质的理解应用,掌握基础是关键,题目较简单.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
5.X、Y、Z是三种气态物质,在一定温度下其变化符合如图所示.下列说法一定正确的是( )
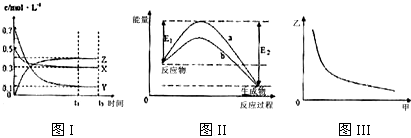

| A. | 该反应热化学方程式为X(g)+3Y(g)?2Z(g)△H=-(E2-E1)kJ•mol-1 | |
| B. | 若图III中甲表示压强,乙表示Z的含量,则其变化符合图III中曲线 | |
| C. | 该温度下,反应的平衡常数数值约为533.若升高温度,该反应的平衡常数减小,Y的转化率降低 | |
| D. | 图II中曲线a是加入催化剂时的能量变化曲线,曲线b是没有加入催化剂时的能量变化曲线 |
12.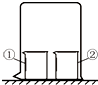 用图所示装置进行下列实验,实验结果与预测现象不一致的是( )
用图所示装置进行下列实验,实验结果与预测现象不一致的是( )
 用图所示装置进行下列实验,实验结果与预测现象不一致的是( )
用图所示装置进行下列实验,实验结果与预测现象不一致的是( )| 选项 | ①中物质 | ②中物质 | 预测现象 |
| A | 酚酞溶液 | 浓氨水 | ①中无色变红色 |
| B | CCl4 | 液溴 | ①中变橙色 |
| C | 浓氨水 | 浓硫酸 | 空气中产生白烟 |
| D | NaAlO2溶液 | 浓盐酸 | ①中有白色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
2.将SO2气体通入BaCl2溶液至饱和,未见沉淀生成,继续通入另一种气体有沉淀产生.则通入的该气体可能是( )
①NO2 ②CO2 ③Cl2 ④HCl ⑤NH3 ⑥H2S.
①NO2 ②CO2 ③Cl2 ④HCl ⑤NH3 ⑥H2S.
| A. | ①②③⑤ | B. | ①④⑤⑥ | C. | ②③⑤⑥ | D. | ①③⑤⑥ |
9.下列说法不正确的是( )
| A. | 在化学反应进行的过程中放出或吸收的热量称为反应热 | |
| B. | 在稀溶液中,1mol酸跟1mol碱发生中和反应所放出的热量叫做中和热 | |
| C. | 氢氧化钡晶体与氯化铵晶体混合是吸热反应 | |
| D. | 化学反应中的能量变化与参加反应的物质的量成正比 |
6.下列实验操作所对应的现象与结论都正确的是( )
| 选项 | 实验操作 | 实验现象 | 绪论 |
| A | 向盛有Fe(NO3)2溶液的试管中加入0.1mol•L-1 H2SO4溶液 | 试管口出现红棕色气体 | 溶液NO3-被Fe2+还原为NO2 |
| B | 溴乙烷中加入氢氧化钠溶液加热充分反应后,滴入硝酸银溶液 | 产生浅黄色沉淀 | 溴乙烷中含有溴元素 |
| C | 在0.1mol•L-1 Na2CO3溶液中,加两滴酚酞显浅红色,微热 | 红色加深 | 盐类水解是吸热反应 |
| D | 向含有硫酸钡沉淀的溶液加入浓碳酸钠溶液,充分搅拌后过滤、洗涤,在滤渣中加入盐酸 | 产生无色无味气体 | Ksp(BaSO4)>Ksp(BaCO3) |
| A. | A | B. | B | C. | C | D. | D |
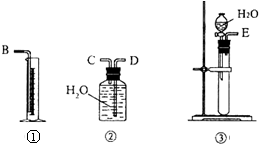 现有含CaO杂质的CaC2试样.某研究性学习小组的同学用图中的装置,设计一个实验,测定CaC2试样的纯度.
现有含CaO杂质的CaC2试样.某研究性学习小组的同学用图中的装置,设计一个实验,测定CaC2试样的纯度.