��Ŀ����
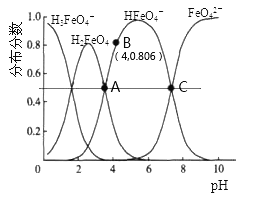
����Ŀ���������(K2FeO4)��һ��������ˮ��������25������ˮ��Һ�м�����ı���Һ��pHʱ���������ӵ����ʵ���������(X)��pH�ı仯��ͼ��ʾ[��֪��(X)= 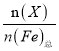 ]������˵����ȷ����
]������˵����ȷ����
A. K2FeO4��H2FeO4������ǿ�����
B. 25����H2FeO4+H+![]() H3FeO4+��ƽ�ⳣ��K>100
H3FeO4+��ƽ�ⳣ��K>100
C. ��B�����ݿ�֪��H2FeO4�ĵ�һ�����볣��Ka1=4.15��10-4
D. A.C �����Ӧ��Һ��ˮ�ĵ���̶�: C
���𰸡�C
��������A����ͼ��֪��H2FeO4�ֲ����룬����������ʡ���A����B����ͼ��֪��25����H2FeO4 + H+![]() H3FeO��ƽ�ⳣ��ԼΪ101.7��100����B����C����B�����ݿ�֪��H2FeO4�ĵ�һ�����볣��Ka1 =
H3FeO��ƽ�ⳣ��ԼΪ101.7��100����B����C����B�����ݿ�֪��H2FeO4�ĵ�һ�����볣��Ka1 =![]() = 4.15 �� 10-4����C��ȷ��D. C��ƫ���ԣ���������pH���ܱ��A�㣬�˹�����ˮ�ĵ��뱻���ƣ�����ˮ�ĵ���̶�C��A����D����ѡC��
= 4.15 �� 10-4����C��ȷ��D. C��ƫ���ԣ���������pH���ܱ��A�㣬�˹�����ˮ�ĵ��뱻���ƣ�����ˮ�ĵ���̶�C��A����D����ѡC��

��ϰ��ϵ�д�
�����Ŀ