题目内容
【题目】某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+和K+。取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol NH3气体(假设生成气体完全逸出),同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6g固体(已知难溶性碱受热易分解,生成相应的金属氧化和水,如 M(OH)n![]() MOn/2+
MOn/2+![]() H2O)向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀。由此可知原溶液中
H2O)向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀。由此可知原溶液中
A.至少存在3种离子
B.CO32-、K+一定不存在
C.SO42-、NH4+、Fe3+一定存在,Cl-可能不存在
D.Cl- 一定存在
【答案】D
【解析】
加入过量NaOH溶液,加热,得到0.02mol气体,可知一定存在NH4+,其物质的量是n(NH4+)=0.02mol,产生的红褐色沉淀是Fe(OH)3,1.6g固体为Fe2O3,可知一定有Fe3+,由于Fe3+与CO32-会发生反应,所以一定没有CO32-,n(Fe2O3)=1.6g÷160g/mol=0.01mol,则根据Fe元素守恒可知n(Fe3+)=2n(Fe2O3)=0.02mol;4.66g不溶于盐酸的沉淀,为BaSO4沉淀,n(BaSO4)=4.66g÷233g/mol=0.02mol,则n(SO42-)=n(BaSO4)= 0.02mol,溶液中存在电荷守恒,NH4+、Fe3+所带正电荷为3n(Fe3+)+n(NH4+)=3×0.02mol+0.02mol=0.08mol,SO42-所带负电荷为2n(SO42-)=2×0.02mol=0.04mol,所以溶液中一定存在阴离Cl-离子。
A.由上述分析可知,一定含SO42-、NH4+、Fe3+、Cl-,所以至少存在四种离子,A错误;
B.由电荷守恒可知,CO32-一定不存在,K+可能有,也可能没有,B错误;
C.由上述分析可知,一定含SO42-、NH4+、Fe3+、Cl-,C错误;
D. 由上述分析可知,一定含Cl-,D正确;
故合理选项是D。

【题目】碱式硫酸铁[Fe(OH)SO4 ]是一种新型高效絮凝剂,常用于污水处理,在医疗上也可用于治疗消化性溃疡出血。工业上利用废铁屑(含少量氧化铝等)生产碱式硫酸铁的工艺流程如下所示:
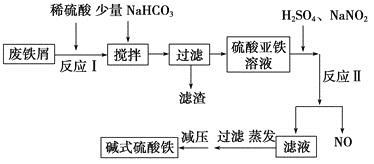
部分阳离子以氢氧化物形式沉淀时溶液的pH如表所示:
沉淀物 | Fe(OH) 3 | Fe(OH) 2 | Al(OH) 3 |
开始沉淀 | 2.3 | 7.5 | 3.4 |
完全沉淀 | 3.2 | 9.7 | 4.4 |
请回答下列问题:
(1)加入少量NaHCO3 的目的是调节溶液的pH,除去Al3+ ,①pH的范围__________,②写出可能发生的离子方程式:________________。
(2)在实际生产中,反应Ⅱ中常同时通入O2 ,以减少NaNO2 的用量,O2 与NaNO2 在反应中均作__________。若参与反应的O2 有11.2 L(标准状况),则相当于节约NaNO2 的物质的量为________。
(3)碱式硫酸铁溶于水后产生的Fe(OH)2+ 可部分水解生成Fe2(OH)42-,该水解反应的离子方程式为________________________________________________________________。 Fe(OH)3 的Ksp =____________。(提示,开始沉淀c(Fe 3+ )浓度为1.0×10 -5 mol/L)
(4)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁。根据我国质量标准,产品中不得含有Fe2+ 及NO3-。为检验所得的产品中是否含有Fe2+ ,应使用的试剂为________。