题目内容
【题目】在密闭容器中的一定量混合气体发生反应:x A(g) + y B(g) ![]() z C(g),平衡时测得A的浓度为0.5 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再次达到平衡时,测得A的浓度降低为0.3 mol/L,下列有关判断正确的是( )
z C(g),平衡时测得A的浓度为0.5 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再次达到平衡时,测得A的浓度降低为0.3 mol/L,下列有关判断正确的是( )
A.x + y < z B.B的转化率降低
C.平衡向正反应方向移动 D.C的体积分数增大
【答案】B
【解析】
试题分析:A、其它条件不变时,将容器的容积扩大到原来的两倍,由![]() 可知A的浓度立即减半,变为0.5 mol/L ÷ 2 = 0.25 mol/L,再次达到平衡时,测得A的浓度降低为0.3 mol/L,说明减小压强能使x A(g) + y B(g)
可知A的浓度立即减半,变为0.5 mol/L ÷ 2 = 0.25 mol/L,再次达到平衡时,测得A的浓度降低为0.3 mol/L,说明减小压强能使x A(g) + y B(g) ![]() z C(g)的平衡向逆反应方向移动,由于减小压强能使平衡向气体物质的量或体积增大方向移动,则逆反应是气体物质的量或体积增大的方向,则x + y > z,A错误;B、由于增大容积的实质是减小压强,减小压强能使平衡向气体物质的量或体积增大的方向移动,即逆向移动,因此反应物B的转化率减小,B正确;C、由上述分析可知,平衡向逆反应方向移动,C错误;D、由于平衡向气体物质的量增大或逆反应方向移动,因此C的物质的量减小,而混合气体总的物质的量增大,因此C的物质的量分数减小,D错误;答案选B。
z C(g)的平衡向逆反应方向移动,由于减小压强能使平衡向气体物质的量或体积增大方向移动,则逆反应是气体物质的量或体积增大的方向,则x + y > z,A错误;B、由于增大容积的实质是减小压强,减小压强能使平衡向气体物质的量或体积增大的方向移动,即逆向移动,因此反应物B的转化率减小,B正确;C、由上述分析可知,平衡向逆反应方向移动,C错误;D、由于平衡向气体物质的量增大或逆反应方向移动,因此C的物质的量减小,而混合气体总的物质的量增大,因此C的物质的量分数减小,D错误;答案选B。

 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案【题目】碳及其含碳化合物在人们的生产生活中应用广泛。
(1)将不同量的CO2(g)和H2(g)分别通入到体积为2L的恒容密闭容器中,进行反应2CO2(g)+6H2(g)CH3CH2OH(g)+3H2O(g),得到如表三组数据;
实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需 时间/min | ||
CO2 | H2 | H2 | C2H5OH | |||
1 | 650 | 2 | 6.8 | 2.0 | 0.8 | 6 |
2 | 900 | 2 | 4.4 | 2.0 | 0.4 | 3 |
3 | 900 | 4 | 8.8 | C | d | t |
①实验1中以v(H2)表示的反应速率为________________
②已知在一定温度下,当一个可逆反应达到化学平衡时,生成物浓度幂之积与反应物浓度幂之积的比值是一个常数称之为化学平衡常数。900℃化学平衡常数为______________,
③如果改变影响平衡的条件之一(如温度,压强,反应物的浓度)平衡将向着能够减弱这种改变的方向移动。则第3组与第2组相比CO2的转化率___________(填“增大”“减小”“不变” 不能确定).
(2)将CH4设计成燃料电池,其利用率更高,装置示意如图(A、B为多孔性碳棒). 持续通入甲烷,在标准状况下,消耗甲烷体积VL.
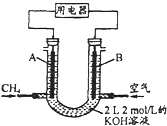
①0<V![]() 44.8L时,负极电极反应为_________________
44.8L时,负极电极反应为_________________
②44.8L<V![]() 89.6L时,电池总反应方程式为_____________
89.6L时,电池总反应方程式为_____________