题目内容
【题目】TMB是一种新型指纹检测的色原试剂,由碳、氢、氮三种元素组成,M=240g/mol。某研究性学习小组的同学欲利用下列仪器测定TMB的分子式。主要过程为在足量氧气流中将4.80 g TMB样品氧化(氮元素转化为N2),再利用吸收剂分别吸收水蒸气和CO2。请从图中选择适当的装置(装置符合气密性要求,加热装置等已略去,其他用品可自选)。
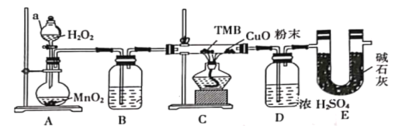
(1)写出仪器a的名称__________,A中的化学反应方程式:___________;
(2)B中试剂是___________,作用是________________ ;
(3)装置C中CuO粉末的作用为________________。
(4)理想状态下,将4.80 gTMB样品完全氧化,点燃C处酒精灯,实验结束时测得D增加3.60 g,E增加14.08 g,则TMB的分子式为____________。
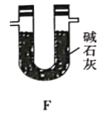
(5)有同学认为,用该实验装置测得的TMB分子式不准确,应在干燥管E后再添加一个装有碱石灰的干燥管F。你认为是否需要添加F装置__________(填“需要”或“不需要”),简述理由________________。
【答案】分液漏斗 ![]() 浓硫酸 干燥 O2,防止将水蒸气带入 D或E 中引起增重 使TMB不充分燃烧生成CO全部转化为CO2 C16H20N2 需要 防止外界空气中的 CO2 和 H2O 进入 E 中,避免对 E 处吸收二氧化碳的定量检测造成干扰
浓硫酸 干燥 O2,防止将水蒸气带入 D或E 中引起增重 使TMB不充分燃烧生成CO全部转化为CO2 C16H20N2 需要 防止外界空气中的 CO2 和 H2O 进入 E 中,避免对 E 处吸收二氧化碳的定量检测造成干扰
【解析】
由实验装置可知,A中过氧化氢在二氧化锰催化作用下生成氧气,B中浓硫酸干燥氧气,C中氧气将TMB氧化为二氧化碳、水和氮气,D中浓硫酸增重为水的质量,E中增重为二氧化碳的质量,结合质量及物质的量计算TMB分子中碳、氢、氮的原子个数比,根据相对分子质量之比算出相对分子质量,结合原子个数比计算出分子式,有必要在干燥管E后再添加一个装有碱石灰的干燥管F,防止空气中的水和二氧化碳进入E,以此解答该题。
(1)由装置图可知,仪器a为分液漏斗, A中发生H2O2在MnO2催化下分解制备氧气,故化学反应方程式为![]() ,故答案为:分液漏斗;
,故答案为:分液漏斗;![]() ;
;
(2)B 中试剂是浓硫酸,作用是干燥O2,防止带入 D或E 中引起增重,故答案为:浓硫酸;干燥O2,防止将水蒸气带入 D或E 中引起增重;
(3)装置C中CuO粉末的作用为使TMB不充分燃烧生成的CO全部转为CO2,故答案为:使TMB不充分燃烧生成CO全部转化为CO2;
(4)实验后称得D、E装置分别增加3.60g、14.08g,则m(H2O)=3.60g,m(CO2)=14.08g,则![]() ,n(H)=2n(H2O)=0.4mol;
,n(H)=2n(H2O)=0.4mol;![]() ,n(C)=n(CO2)=0.32mol;
,n(C)=n(CO2)=0.32mol;
所以![]() ;
;
则:n(C):n(H):n(N)=0.32mol:0.4mol:0.04mol=8:10:1,
TMB的相对分子质量为240,设分子式为C8nH10nNn,则有12×8n+10n+14n=240,解得n=2,所以分子式为C16H20N2,故答案为:C16H20N2;
(5)本实验是通过TMB完全燃烧,并利用D、E装置分别吸收H2O和CO2来确定其分子组成,若不添加F装置,外界空气中的CO2和H2O进入E中,从而干扰 E处吸收二氧化碳的定量检测,给实验造成误差,故答案为:需要;防止外界空气中的CO2和H2O进入E 中,避免对 E 处吸收二氧化碳的定量检测造成干扰。