题目内容
现有两份体积相同的混合溶液,其组成如下:
| | KCl | K2SO4 | ZnSO4 | ZnCl2 |
| (1) | 0.4 mol | 0.1mol | 0.3mol | 0.1mol |
| (2) | 0.2mol | 0.2mol | 0.1mol | 0.1mol |
则两份溶液中各离子浓度( )
A. 仅c(K+)相同 B. 仅c(Cl-)相同 C. 完全相同 D. 完全不同
A
解析试题分析:(1)溶液中个离子物质的量为:K+:0.4mol+2×0.1mol=0.6mol,Zn2+:0.3mol+0.1mol=0.4mol,Cl?:0.4mol+2×0.1mol=0.6mol,SO42?:0.1mol+0.3mol=0.4mol;(2)溶液中离子物质的量为:K+:0.2mol+2×0.2mol=0.6mol,Zn2+:0.1mol+0.1mol=0.2mol,Cl?:0.2mol+2×0.1mol=0.4mol,SO42?:0.2mol+0.1mol=0.3mol,所以只有c(Cl?)相同,A项正确。
考点:本题考查离子浓度的计算。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
用NA表示阿伏加德罗常数的值。下列叙述中正确的是( )
| A.标准状况下,0.1 mol Cl2溶于水,转移的电子数目为0.1NA |
| B.标准状况下,33.6 L氟化氢中含有氟原子的数目为1.5NA |
| C.常温常压下,92 g的NO2和N2O4混合气体含有的原子数为6NA |
| D.10 mL质量分数为98%的H2SO4溶液,用水稀释至100 mL,H2SO4的质量分数为9.8% |
下列各组物质中分子数相同的是
| A.2LCO和2LCO2 |
| B.9gH2O和标准状况下11.2LCO2 |
| C.标准状况下1molO2和22.4LH2O |
| D.0.2molH2和4.48LHCl气体 |
设NA为阿伏伽德罗常数的数值,下列说法正确的是
| A.常温下,23g NO2含有NA个氧原子 |
| B.标准状况下,11.2L SO3中含有的分子数为0.5NA |
| C.1 mol Cl2做氧化剂转移的电子数是NA |
| D.1L 0.1mol?L-1的氨水中含OH―离子数为0.1NA个 |
用NA表示阿伏加德罗常数,下列说法正确的是:
| A.用含0.1mol FeCl3的溶液与足量沸水反应制得的Fe(OH)3胶体中胶粒数为0.1NA |
| B.13gNO2和33gN2O4混合气体中含N原子数为NA |
| C.28gCO和22.4LN2含有的分子数均为NA |
| D.等物质的量的NH4+和OH-含电子数均为10NA |
用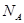 表示阿伏加德罗常数的值。下列叙述中不正确的是
表示阿伏加德罗常数的值。下列叙述中不正确的是
A.足量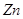 与一定量的浓硫酸反应,产生 与一定量的浓硫酸反应,产生 (标况)气体时,转移的电子数为 (标况)气体时,转移的电子数为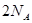 |
B.一定条件下,32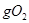 和足量的铁粉充分反应,转移的电子数为 和足量的铁粉充分反应,转移的电子数为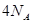 |
C.4.6g乙醇和甲酸(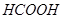 )的混合物中含有的碳原子数在 )的混合物中含有的碳原子数在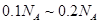 之间 之间 |
D.分子总数为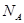 的NO和 的NO和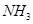 混合气体中含有的氮原子数为 混合气体中含有的氮原子数为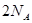 |
NA为阿伏伽德罗常数的值。下列叙述正确的是
| A.将28 g Fe投人到1 Ll mol/L的硫酸中,可得到11.2 LH2 |
| B.常温常压下,64 gSO2气体含有的原子数目为3 NA |
| C.25℃时pH =13的NaOH溶液中含有OH一的数目为0. 1 NA |
| D.1 mo1N a被完全氧化生成Na2O2,失去2 NA个电子 |
下列物质的电子式书写正确的是
A.N2: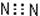 |
B.CO2: |
C.Na2O: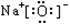 |
D.HCl: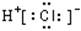 |
下列说法正确的是(NA表示阿伏加德罗常数的值)
| A.常温常压下,18g NH4+所含的电子数为10NA |
| B.56g金属铁与氯气反应时得到的电子数为3NA |
| C.标准状态下,22.4L氧气所含的氧原子数为2 NA |
| D.1 mol由Na2O2和Na2O组成的混合物,其中的钠离子数为4 NA |