题目内容
19.用NA表示阿伏加德罗常数的值,下列说法正确的是( )| A. | 24.5L氢气中所含氢原子数一定大于2NA | |
| B. | 1molCH3+电子数为9NA | |
| C. | 100g 60%CH3COOH水溶液中含有的分子数为NA | |
| D. | 常温常压下0.1mol CO和NO的混合气体含氧原子数为0.1NA |
分析 A、氢气的状态不明确;
B、CH3+中含8个电子;
C、CH3COOH为弱电解质,在溶液中部分电离,且溶液中还存在水分子;
D、CO和NO中均含1个氧原子.
解答 解:A、氢气的状态不明确,故氢气的物质的量不能计算,则含有的氢原子的个数无法计算,故A错误;
B、CH3+中含8个电子,故1molCH3+中含8mol电子即8NA个,故B错误;
C、CH3COOH为弱电解质,在溶液中部分电离,故溶液中的醋酸分子的个数小于NA个,但由于溶液中还存在水分子,故溶液中的分子个数无法计算,故C错误;
D、CO和NO中均含1个氧原子,故0.1molNO和CO中含0.1mol氧原子即0.1NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
9.常温下0.1mol•L-1醋酸溶液的pH=a,下列能使溶液pH=(a+1)的措施是( )
| A. | 将溶液稀释到原体积的10倍 | B. | 加入适量的CH3COONa固体 | ||
| C. | 加入等体积0.2 mol•L-1盐酸 | D. | 提高溶液的温度 |
10.下列气体中所含原子数最多的是( )
| A. | 标准状况下44.8L H2 | B. | 88gCO2 | ||
| C. | 9.03ⅹ1023个CH4 分子 | D. | 3molH2O |
7.下列物质的除杂方案正确的是( )
| 选项 | 被提纯的物质 | 杂质 | 除杂试剂 | 除杂方法 |
| A | CO2 (g) | SO2(g) | 饱和Na2CO3溶液、浓H2SO4 | 洗气 |
| B | NH4Cl(aq) | Fe3+(aq) | NaOH溶液 | 过滤 |
| C | NaCl(s) | KNO3(s) | AgNO3溶液 | 过滤 |
| D | Cu(s) | Ag(s) | CuSO4溶液 | 电解法 |
| A. | A | B. | B | C. | C | D. | D |
11.下列说法正确的是( )
| A. | 可用CCl4和双氧水检验溶液中是否含有I- | |
| B. | 可用漂白粉消毒的自来水配制Na2S03溶液 | |
| C. | 可用KI淀粉溶液鉴别NO2和溴蒸气 | |
| D. | 可用水吸收NO气体 |
8.一般情况下胶体稳定,胶体微粒不易聚集,主要原因是( )
| A. | 胶体粒子因吸附带电荷离子而带同种电荷 | |
| B. | 胶体有布朗运动 | |
| C. | 胶体粒子直径在1~100nm之间,粒子小,不受重力作用 | |
| D. | 胶体有丁达尔现象 |
9.工业上合成尿素的反应为:2NH3(g)+CO2(g)?CO(NH2)2(s)+H2O(g).在一定温度和压强下,往容积可变的密闭容器内通入物质的量各为1mol的氨气和二氧化碳发生上述反应.下列说法中无法判断该反应一定达到化学平衡的是( )
| A. | 打断$\frac{a}{3}$mol的N-H键同时消耗$\frac{a}{6}$mol的尿素 | |
| B. | 密闭容器中混合气体的平均摩尔质量保持不变 | |
| C. | 密闭容器中混合气体的密度保持不变 | |
| D. | 密闭容器中二氧化碳的体积分数保持不变 |
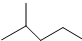 表示的分子式C6H14;名称是2-甲基戊烷,核磁共振氢谱中有5组峰.
表示的分子式C6H14;名称是2-甲基戊烷,核磁共振氢谱中有5组峰.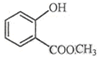 中含有的官能团的名称为羟基、酯基.
中含有的官能团的名称为羟基、酯基.