题目内容
9.常温下0.1mol•L-1醋酸溶液的pH=a,下列能使溶液pH=(a+1)的措施是( )| A. | 将溶液稀释到原体积的10倍 | B. | 加入适量的CH3COONa固体 | ||
| C. | 加入等体积0.2 mol•L-1盐酸 | D. | 提高溶液的温度 |
分析 醋酸电离生成醋酸根离子和氢离子,要使溶液的pH增大,则溶液中氢离子浓度减小,据此分析解答.
解答 解:A、醋酸是弱电解质,加水稀释能促进水的电离,将溶液稀释到原体积的10倍,氢离子浓度大于原来的$\frac{1}{10}$,所以pH<(a+1),故A错误;
B、加入适量的醋酸钠固体,醋酸钠中含有醋酸根离子能抑制醋酸的电离,使溶液中氢离子浓度减小,所以能使溶液pH=(a+1),故B正确;
C、加入等体积的0.2 mol•L-1盐酸,氢离子浓度增大,溶液的pH值减小,故C错误;
D、提高温度促进醋酸的电离,使溶液中氢离子浓度增大,溶液的pH值减小,故D错误;
故选B.
点评 本题考查了弱电解质的电离,根据“加水稀释、提高温度都能促进醋酸的电离,加入含有相同离子的盐能抑制醋酸的电离”来分析解答,难度不大.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
20.某实验小组设计实验测定Na2S04和Na2C03混合物中各组分的含量.
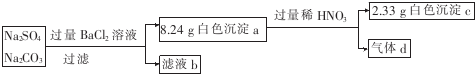
下列说法不正确的是( )

下列说法不正确的是( )
| A. | 沉淀a的主要成分是BaS04和BaC03 | |
| B. | 滤液b中Na+的物质的量为0.08 mol | |
| C. | 气体d在标准状况下的体积为224 mL | |
| D. | 原混合物中Na2S04与Na2C03的物质的量之比为1:3 |
17.某小组用如图装置进行实验,下列说法正确的是( )


| A. | 盐桥中的电解质可以用KC1 | |
| B. | 导线中流过0.2mol电子时,加入4.9gCu(OH)2,CuSO4溶液可恢复原组成 | |
| C. | 闭合K,石墨电极上只生成铜 | |
| D. | 闭合K,外电路电流方向为Fe电极→石墨电极 |
4.下列实验操作中错误的是( )
| A. | 蒸发操作时,当溶液中出现较多固体应停止加热 | |
| B. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 如果没有试管夹,可以临时手持试管给固体或液体加热 |
1.下列物质所属的类别及其所含官能团的对应关系不正确的是( )
| A. | CH3CH=CH2 烯烃 | B. |  羧酸-COOH 羧酸-COOH | ||
| C. |  醛类 醛类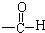 | D. | RCH2OH (R为烃基) 醇类-OH |
19.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 24.5L氢气中所含氢原子数一定大于2NA | |
| B. | 1molCH3+电子数为9NA | |
| C. | 100g 60%CH3COOH水溶液中含有的分子数为NA | |
| D. | 常温常压下0.1mol CO和NO的混合气体含氧原子数为0.1NA |

 、B
、B 、C
、C 、F
、F ;
; +2H2O.
+2H2O.