题目内容
4.(1)键线式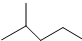 表示的分子式C6H14;名称是2-甲基戊烷,核磁共振氢谱中有5组峰.
表示的分子式C6H14;名称是2-甲基戊烷,核磁共振氢谱中有5组峰.(2)
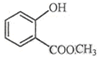 中含有的官能团的名称为羟基、酯基.
中含有的官能团的名称为羟基、酯基.(3)(CH3)3CCHOHCH3名称为3,3-二甲基-2-戊醇.
分析 (1)根据该有机物的键线式写出分子式,根据系统命名法完成该有机物的命名;核磁共振氢谱中峰值数等于有机物中氢原子的种类数;
(2)根据有机物的结构写出分子中含有的官能团;
(3)根据系统命名法完成该有机物的命名.
解答 解:(1)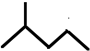 ,分子中含有6个碳原子,属于饱和烃,分子式为C6H14,该有机物主链上有5个C,2号C一个甲基,命名为:2-甲基戊烷;
,分子中含有6个碳原子,属于饱和烃,分子式为C6H14,该有机物主链上有5个C,2号C一个甲基,命名为:2-甲基戊烷; 有5种H原子,核磁共振氢谱中有5个峰;
有5种H原子,核磁共振氢谱中有5个峰;
故答案为:C6H14; 2-甲基戊烷;5;
(2) 分子中含有官能团是羟基和酯基,故答案为:羟基、酯基;
分子中含有官能团是羟基和酯基,故答案为:羟基、酯基;
(3)该有机物主链上有5个C,羟基在2号位,3号C有3个甲基,命名为:3,3-二甲基-2-戊醇,故答案为:3,3-二甲基-2-戊醇.
点评 本题考查有机物分子式的书写、官能团的判断、以及有机物的命名,难度不大.要求学生了解有机物的系统命名方法,熟练掌握常见的官能团名称.

练习册系列答案
相关题目
15.下列混合溶液中,各离子浓度的大小顺序正确的是( )
| A. | 10mL0.5mol/LCH3COONa溶液与6mL1mol/L盐酸混合c(Clˉ)>c(Na+)>c(OHˉ)>c(H+) | |
| B. | 10mL0.1mol/LNH4 Cl溶液与5mL0.2mol/LNaOH溶液混合c(Na+)=c(Clˉ)>c(OHˉ)>c(H+) | |
| C. | 10mL0.1mol/LCH3COOH溶液与5mL0.2mol/LNaOH溶液混合c(Na+)=c(CH3COOˉ)>c(OHˉ)>c(H+) | |
| D. | 10mL0.1mol/L氨水与10mL0.1mol/L盐酸混合 c(Clˉ)>c(NH4+)>c(OHˉ)>c(H+) |
12. 如图两个装置中,液体体积均为200mL,开始工作前电解质溶液的浓度均为0.5mol/L,工作一段时间后,测得有0.02mol电子通过,若忽略溶液体积的变化,下列叙述正确的是( )
如图两个装置中,液体体积均为200mL,开始工作前电解质溶液的浓度均为0.5mol/L,工作一段时间后,测得有0.02mol电子通过,若忽略溶液体积的变化,下列叙述正确的是( )
 如图两个装置中,液体体积均为200mL,开始工作前电解质溶液的浓度均为0.5mol/L,工作一段时间后,测得有0.02mol电子通过,若忽略溶液体积的变化,下列叙述正确的是( )
如图两个装置中,液体体积均为200mL,开始工作前电解质溶液的浓度均为0.5mol/L,工作一段时间后,测得有0.02mol电子通过,若忽略溶液体积的变化,下列叙述正确的是( )| A. | 产生气体体积 ①=② | |
| B. | ①中阴极质量增加,②中正极质量减小 | |
| C. | 溶液的H+浓度变化:①增大,②减小 | |
| D. | 电极反应式①中阳极:4OH--4e-═2H2O+O2↑,②中负极:2H++2e-═H2↑ |
19.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 24.5L氢气中所含氢原子数一定大于2NA | |
| B. | 1molCH3+电子数为9NA | |
| C. | 100g 60%CH3COOH水溶液中含有的分子数为NA | |
| D. | 常温常压下0.1mol CO和NO的混合气体含氧原子数为0.1NA |
9.常温下;在指定环境中,下列各组离子一定能大量共存的是( )
| A. | 使pH试纸呈红色的溶液中:I-、Cl0-、S032-、Na+ | |
| B. | 1.0 mol/L的KNO3溶液中:H+、Fe2+、Cl-、S042- | |
| C. | 由水电离出的C(H+)=10-13mol/L的溶液中:C032-、S042-、Cl-、Na+ | |
| D. | 在含有大量HC03-的溶液中:K+、Ba2+、Cl-、N03- |
16.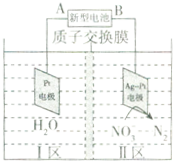 以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,通过电解原理来降解酸性废水中的NO3-,下列说法错误的是( )
以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,通过电解原理来降解酸性废水中的NO3-,下列说法错误的是( )
 以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,通过电解原理来降解酸性废水中的NO3-,下列说法错误的是( )
以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,通过电解原理来降解酸性废水中的NO3-,下列说法错误的是( )| A. | 该新型电池工作时,负极的电极反应式是Al+4OH--3e-═AlO2-+2H2O | |
| B. | 为增强溶液的导电性,I区水中可加入少量Na2SO4 | |
| C. | A为电源正极,H+从Ⅰ区移向Ⅱ区 | |
| D. | 阴极反应式为:2NO3-+6H2O+10e-═N2↑+12OH- |
13.下列说法正确的是( )
| A. | KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 | |
| B. | HClO是弱酸,所以NaClO是弱电解质 | |
| C. | HCl溶液和NaCl溶液均通过离子导电,所以HCl和NaCl均是离子化合物 | |
| D. | BaSO4 和NaHCO3都是强电解质 |
14.某校实验室将药品分类后放在不同的药品柜里,巳存放的部分药品如下.该实验室新购进部分生石灰和纯碱应将它们分别放在( )
| 药品柜编号 | ① | ② | ③ | ④ | … |
| 药品 | 氢氧化钠 氢氧化钙 | 盐酸 硫酸 | 二氧化锰 氧化铜 | 氯化钠 硫酸钠 | … |
| A. | ③和① | B. | ④和① | C. | ①和② | D. | ③和④ |