题目内容
14.人造地球卫星用到的一种高能电池--银锌蓄电池,其电池的电极反应式为:Zn+2OH--2e-═ZnO+H2↑,Ag2O+H2O+2e═2Ag+2OH-.据此判断正确的是( )| A. | Zn负极,并被还原 | B. | Ag2O正极,并被还原 | ||
| C. | 电解质溶液为碱性 | D. | Zn正极,并被氧化 |
分析 根据化合价变化可知Zn被氧化,应为原电池的负极,则正极为Ag2O,正极上得电子被还原,根据Zn+2OH--2e-═ZnO+H2↑,则电解质溶液为碱性,据此分析.
解答 解:A、根据化合价可知,Zn被氧化,应为原电池的负极,故A错误;
B、正极为Ag2O,正极上得电子被还原,故B正确;
C、根据Zn+2OH--2e-═ZnO+H2↑,则电解质溶液为碱性,故C正确;
D、Zn被氧化,应为原电池的负极,故D错误.
故选BC.
点评 本题考查原电池知识,题目难度中等,注意原电池两极上的变化以及原电池原理.

练习册系列答案
相关题目
5.随着化石能源的日益减少,能源危机成为目前人类面临的重要问题.主要利用化学方法产生新能源的事例为( )
| A. | 风力发电 | B. | 潮汐能发电 | ||
| C. | 水力发电 | D. | 太阳能光解水制取H2 |
2.某主族元素的最高价含氧酸的阴离子的符号是RO3-,则该元素的气态氢化物的化学式是( )
| A. | HR | B. | H2R | C. | RH3 | D. | RH4 |
19.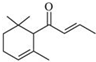 一种从植物中提取的天然化合物α-damascone可用于制作“香水”,其结构为:,有关该化合物的下列说法不正确的是( )
一种从植物中提取的天然化合物α-damascone可用于制作“香水”,其结构为:,有关该化合物的下列说法不正确的是( )
 一种从植物中提取的天然化合物α-damascone可用于制作“香水”,其结构为:,有关该化合物的下列说法不正确的是( )
一种从植物中提取的天然化合物α-damascone可用于制作“香水”,其结构为:,有关该化合物的下列说法不正确的是( )| A. | 分子式为C13H20O | |
| B. | 该化合物可发生聚合反应 | |
| C. | 与溴的CCl4溶液反应生成的产物经水解、稀硝酸酸化后可用AgNO3溶液检验 | |
| D. | 1 mol该化合物完全燃烧消耗19 molO2 |
4.下列说法或表示方法中正确的是( )
| A. | 全部由非金属元素组成的化合物中只含共价键 | |
| B. | 燃料电池的能量转化率可达100% | |
| C. | 已知C(s,石墨)=C(s,金刚石)△H=+1.9 kJ/mol,则石墨比金刚石稳定 | |
| D. | 氢气的燃烧热为285.8 kJ/mol,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ/mol |



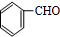 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2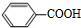 .
.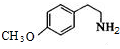 .
. .
.