题目内容
4.下列说法或表示方法中正确的是( )| A. | 全部由非金属元素组成的化合物中只含共价键 | |
| B. | 燃料电池的能量转化率可达100% | |
| C. | 已知C(s,石墨)=C(s,金刚石)△H=+1.9 kJ/mol,则石墨比金刚石稳定 | |
| D. | 氢气的燃烧热为285.8 kJ/mol,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ/mol |
分析 A、全部由非金属元素组成的化合物中可能含有离子键;
B、原电池原理分析,化学能转化为电能过程中伴随热量转化;
C、物质能量越高越活泼;
D、燃烧热是1mol可燃物完全燃烧生成稳定氧化物时放出的热量.
解答 解:A、全部由非金属元素组成的化合物中可能含有离子键,如铵盐,故A错误;
B、燃料电池中还有部分化学能转化为热能,所以能量转化率不是100%,故B错误;
C、C(s,石墨)=C(s,金刚石)△H=+1.9 kJ/mol,金刚石能量高活泼,则石墨比金刚石稳定,故C正确;
D、氢气的燃烧热为285.8 kJ/mol,则氢气燃烧的热化学方程式为:H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8 kJ/mol,故D错误;
故选C.
点评 本题考查了化学反应能量变化,热化学方程式书写,燃烧热概念的理解应用,掌握基础是关键,题目较简单.

练习册系列答案
 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
14.人造地球卫星用到的一种高能电池--银锌蓄电池,其电池的电极反应式为:Zn+2OH--2e-═ZnO+H2↑,Ag2O+H2O+2e═2Ag+2OH-.据此判断正确的是( )
| A. | Zn负极,并被还原 | B. | Ag2O正极,并被还原 | ||
| C. | 电解质溶液为碱性 | D. | Zn正极,并被氧化 |
15.下列实验操作正确的是( )
| A. | 在催化剂存在的条件下,苯和溴水发生反应可生成无色、比水重的液体溴苯 | |
| B. | 配制银氨溶液时,将稀氨水慢慢滴入硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止 | |
| C. | 醇中含有少量水可加入硫酸铜再蒸馏制得无水乙醇 | |
| D. | 验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合,充分振荡溶液、静置、待液体分层后,滴加硝酸银溶液 |
12.下列实验现象预测正确的是( )
| A. | 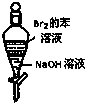 如图实验:振荡后静置,上层溶液颜色保持不变 如图实验:振荡后静置,上层溶液颜色保持不变 | |
| B. | 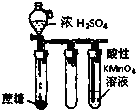 如图实验:酸性KMnO4溶液中出现气泡,且颜色逐渐褪去 如图实验:酸性KMnO4溶液中出现气泡,且颜色逐渐褪去 | |
| C. | 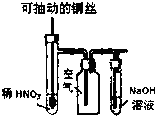 如图实验Ⅲ:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 如图实验Ⅲ:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 | |
| D. | 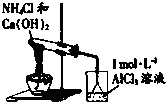 如图实验IV:烧杯中先出现白色沉淀,后溶解 如图实验IV:烧杯中先出现白色沉淀,后溶解 |
19.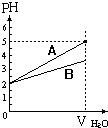 pH值等于2的两种酸溶液A和B,分别加水稀释1000倍,其pH值与所加水的体积变化趋势示意图如图所示,则下列结论正确的是:( )
pH值等于2的两种酸溶液A和B,分别加水稀释1000倍,其pH值与所加水的体积变化趋势示意图如图所示,则下列结论正确的是:( )
 pH值等于2的两种酸溶液A和B,分别加水稀释1000倍,其pH值与所加水的体积变化趋势示意图如图所示,则下列结论正确的是:( )
pH值等于2的两种酸溶液A和B,分别加水稀释1000倍,其pH值与所加水的体积变化趋势示意图如图所示,则下列结论正确的是:( )| A. | 等体积pH=2的两种酸中和NaOH的能力酸A比酸B强 | |
| B. | A为弱酸,B为强酸 | |
| C. | 酸B的摩尔浓度比酸A大 | |
| D. | A比B易电离 |
16.硬水中含有较多可溶性钙、镁化合物,为降低水的硬度,下列方法可行的是( )
| A. | 煮沸 | B. | 静置 | C. | 过滤 | D. | 吸附 |
13.如图所示,在用锌片、铜片和稀硫酸组成的原电池装置中,下列说法正确的是( )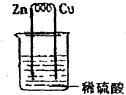

| A. | 铜片上的反应为:Cu-2e-=Cu2+ | B. | 锌片上的反应为:2H++2e-=H2↑ | ||
| C. | 锌片是负极,铜片是正极 | D. | 反应一段时间后,溶液的pH变小 |
14.下列各组离子,在水溶液中不能大量共存的是( )
| A. | H+、K+、Cl-、NO3- | B. | K+、A13+、Cl-、AlO2- | ||
| C. | Na+、K+、CO32-、NO3- | D. | A13+、Cu2+、SO42-、I- |