题目内容
20.下列化合物中只含有离子键的是( )| A. | KOH | B. | H2O | C. | CaCl2 | D. | NH3 |
分析 一般来说,活泼金属和活泼非金属元素之间存在离子键,非金属元素之间存在共价键,据此分析解答.
解答 解:A.氢氧化钾中钾离子和氢氧根离子之间存在离子键,氧原子和氢原子之间存在共价键,故A错误;
B.水中氧原子和氢原子之间存在共价键,故B错误;
C.CaCl2是离子化合物,钙离子和氯离子之间存在离子键,故C正确;
D.氨气中只含共价键,故D错误;
故选C.
点评 本题考查了化学键的判断,难度不大,注意由金属元素和非金属元素形成的化合物不一定是离子化合物,如氯化铝是共价化合物,为易错点.

练习册系列答案
相关题目
8.设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | 常温常压下,22.4L氧气与金属钠完全反应,转移的电子数一定是4NA | |
| B. | 常温常压下,1.7gH2O2中含有电子数为0.9NA | |
| C. | 1L 0.2 mol•L-1 FeCl3溶液中,含有Fe3+粒子数为0.2 NA | |
| D. | 标准状况下,0.1mol 甲苯所含C-C键数为0.6NA |
15.下列说法正确的是( )
| A. | 大分子化合物油脂在人体内水解为氨基酸和甘油等小分子才能被吸收 | |
| B. | 硫酸厂按照规定已经处理除去了重金属离子的酸性废水,可直接排放入湖水中 | |
| C. | 现代科技已经能够拍到氢键的“照片”,直观地证实了水分子间的氢键是一个水分子中的氢原子与另一个水分子中的氧原子间形成的化学键 | |
| D. | 合金超导材料是指熔合两种或两种以上的金属元素并形成具有超导电性的超导材料,如铌一钛(Nb-Ti)合金,它的熔点一般比纯钛要低 |
5.出去下列各组物质中的杂质(括号内为杂质),采用方法不正确的是( )
| A. | NaCl(NH4Cl):加热 | B. | FeCl2(FeCl3):铁粉 | ||
| C. | AlCl3(MgCl2):加氨水 | D. | Fe2O3(Al2O3):加氢氧化钠溶液 |
12.对于可逆反应M+N?P+Q,有关说法正确的是( )
| A. | 使用催化剂能改变反应限度 | |
| B. | 升高温度,则反应速率减慢 | |
| C. | 四种物质的量浓度相等时,则一定达到了该反应的限度 | |
| D. | 各物质的浓度不再发生变化时,则达到化学反应的限度 |
9.下列过程发生化学变化的是( )
| A. | 酒香扑鼻 | B. | 蜡烛照明 | ||
| C. | 用金刚石切割玻璃 | D. | 太阳能供热 |
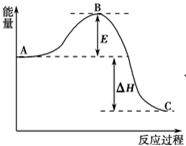 2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ•mol-1.请回答下列问题:
2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ•mol-1.请回答下列问题: