题目内容
17.室温下,pH均为13的Na2CO3和NaOH溶液中,水电离产生的c(OH-)之比=1012.分析 氢氧化钠为强碱溶液,氢氧根离子抑制了水的电离,溶液中氢离子是水电离的;碳酸钠溶液中,碳酸根离子水解促进了水的电离,溶液中氢氧根离子为水电离的,据此进行判断.
解答 解:25℃时,pH=13的碳酸钠溶液中,碳酸根离子水解促进了水的电离,溶液中氢氧根离子是水电离的,水电离的氢离子和氢氧根浓度均为:$\frac{1×1{0}^{-14}}{1×1{0}^{-13}}$mol/L=1×10-1mol/L;
pH值等于13的NaOH溶液中,氢氧根离子抑制了水的电离,溶液中氢离子是水电离的,水电离的氢离子和氢氧根浓度均为:1×10-13mol/L;
,故Na2CO3和NaOH溶液中溶液中水电离产生的c(OH-)之比1012.
故答案为:1012.
点评 本题考查水的电离及其影响因素,难度不大.注意明确酸溶液、碱溶液抑制水的电离,能够水解的盐溶液促进水的电离.

练习册系列答案
相关题目
5.短周期原子序数依次增大的主族元素R、T、Q、W、Y具有如下信息:①R、Y原子的最外层电子数与电子层数相同;②Q的最外层电子数是次外层的3倍,R与T的核电荷数之和等于Q的核电荷数;③W与R最外层电子数相同.下列说法正确的是( )
| A. | 元素T、Q、W、Y的原子半径大小为:T<Q<Y<W | |
| B. | 元素Q与W形成的两种常见化合物中含有相同比例的阴、阳离子 | |
| C. | Q与Y组成的常见物质是一种两性物质,结构中含有共价键 | |
| D. | 由Y和T组成的物质YT,在电子和陶瓷工业上有广泛应用,可以直接由单质Y和T在低温下合成 |
12.下列说法正确的是( )
| A. | 标准状况下44.8L乙醇含有氢原子数为12NA | |
| B. | 1mol气体的体积只有在标准状况下才是22.4L | |
| C. | 常温常压下,等质量的N2和N4中所含氮原子数相同 | |
| D. | 标准状况下1.12L CO和N2的混合气体含有约3.01×1022个原子 |
2.现有常温下的四种溶液:①pH=11的氨水、②0.001mol/L的NaOH溶液、③pH=3的醋酸、④由水电离出的c(H+)=10-11mol/L的盐酸.下列有关叙述正确的是( )
| A. | 分别加水稀释10倍,四种溶液的pH:①>②>④>③ | |
| B. | 将③、④分别稀释到pH=5,由水电离出氢离子的浓度均减小100倍 | |
| C. | 在①、②中分别加入适量的氯化铵晶体后,①的pH减小,②的pH不变 | |
| D. | 将①、④两种溶液等体积混合,所得溶液中:c(OH-):c(H+)<1 |
9.常温时,将a1mL,b1mol/L 的CH3COOH溶液加入到a2mL,b2mol/L 的NaOH溶液中,下列结论中不正确的是( )
| A. | 如果a1b1=a2b2,则混合溶液的pH>7 | |
| B. | 如果混合液的pH=7,则混合溶液中c(CH3COO-)=c(Na+) | |
| C. | 如果a1=a2,b1=b2,则混合液液中c(CH3COO-)=c(Na+) | |
| D. | 如果a1=a2,且混合溶液的pH<7,则b1>b2 |
6. 氮元素的单质及其化合物的研究和应用在工农业生产中有着非常重要的地位.工业制硝酸的主要反应之一是
氮元素的单质及其化合物的研究和应用在工农业生产中有着非常重要的地位.工业制硝酸的主要反应之一是
4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-akJ.mol-1(a>0)
(1)如果将4mol NH3和5molO2放入容器中,达到平衡
时放出热量0.8akJ,则平衡时NH3的转化率为80%.
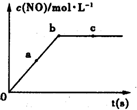
(2)在一定条件下,容积固定的密闭容器中进行上述反应,NO的浓
度与时间关系如图所示,则NO的a、b、c三点的反应速率
v(a正)、v(b逆)、v(c正)的大小关系是v(a正)<v(b逆)=v(c正).
(3)t℃时,在容积固定的密闭容器中发生上述反应,容器内各物质的浓度如下表:
A.第2min时改变了条件,改变的条件可能D.(从所给选项中选择);
A.降低温度 B.增加了生成物 C.减小压强 D.使用了高效催化剂
B.在与第4min相同的温度下,若起始向容器中加入NH3、O2、NO和H2O(g)的浓度为2moI/L,则该反应正反应方向进行.(填“正反应方向进行”、“逆反应方向进行”、“不移动”).
(4)目前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为:
CH4(g)+4NO2(g)=4NO(g)+CO2+2H2O(g)△H=-574KJ.mol-1
CH4+(g)4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160KJ.mol-1
则1mol甲烷直接将NO2还原为N2的焓变为-867kJ•mol-1.
 氮元素的单质及其化合物的研究和应用在工农业生产中有着非常重要的地位.工业制硝酸的主要反应之一是
氮元素的单质及其化合物的研究和应用在工农业生产中有着非常重要的地位.工业制硝酸的主要反应之一是4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-akJ.mol-1(a>0)
(1)如果将4mol NH3和5molO2放入容器中,达到平衡
时放出热量0.8akJ,则平衡时NH3的转化率为80%.
(2)在一定条件下,容积固定的密闭容器中进行上述反应,NO的浓
度与时间关系如图所示,则NO的a、b、c三点的反应速率
v(a正)、v(b逆)、v(c正)的大小关系是v(a正)<v(b逆)=v(c正).
(3)t℃时,在容积固定的密闭容器中发生上述反应,容器内各物质的浓度如下表:
| 浓度/mol.l-1 | C(NH3) | C(O2) | C(NO) | C(H2O) |
| 时间/min | ||||
| 起始 | 4.0 | 5.5 | 0 | 0 |
| 第2min | 3.2 | 4.5 | 0.8 | 1.2 |
| 第4min | 2.0 | 3.0 | 2.0 | 3.0 |
| 第6min | 3.0 | 3.0 | 2.0 | 3.0 |
A.降低温度 B.增加了生成物 C.减小压强 D.使用了高效催化剂
B.在与第4min相同的温度下,若起始向容器中加入NH3、O2、NO和H2O(g)的浓度为2moI/L,则该反应正反应方向进行.(填“正反应方向进行”、“逆反应方向进行”、“不移动”).
(4)目前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为:
CH4(g)+4NO2(g)=4NO(g)+CO2+2H2O(g)△H=-574KJ.mol-1
CH4+(g)4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160KJ.mol-1
则1mol甲烷直接将NO2还原为N2的焓变为-867kJ•mol-1.