题目内容
下列实验能达到预期目的的是
| 编号 | 实验内容 | 实验目的 |
| A | 取两只试管,分别加入4ml 0.01mol/L KMnO4酸性溶液,然后向一只试管中加入0.1mol/L H2C2O4溶液2ml,向另一只试管中加入0.1mol/L H2C2O4溶液4ml,记录褪色时间。 | 可以证明H2C2O4浓度越大反应速率越快。 |
| B | 向1ml 0.2mol/L NaOH溶液中滴入2滴0.1mol/L MgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol/L FeCl3溶液,又生成红褐色沉淀。 | 可以证明在相同温度下,溶解度Mg(OH)2>Fe(OH)3 |
| C | 测定等物质的量浓度的Na2SO3与Na2CO3溶液的pH,后者较大。 | 证明了非金属性S>C |
| D | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色会变浅。 | 可以证明Na2CO3溶液中存在水解平衡。 |
D
试题分析:A、两只试管中草酸的浓度几乎是相同的,所以不能证明H2C2O4浓度越大反应速率越快,A不正确;B、由于氢氧化钠在和氯化镁溶液反应时氢氧化钠过量,所以再加入氯化铁时一定产生红褐色氢氧化铁沉淀,所以不能证明在相同温度下溶解度Mg(OH)2>Fe(OH)3,B不正确;S元素的最高价是+6价,因此应该测定等物质的量浓度的Na2SO4与Na2CO3溶液的pH,如果后者较大可以证明非金属性S>C,C不正确;D、向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色会变浅,这说明溶液中OH-浓度降低,这是由于碳酸钠与氯化钡反应生成了碳酸钡沉淀,从而抑制了CO32-的水解,溶液的碱性降低,D正确,答案选D。

练习册系列答案
相关题目
 [Cu(NH3)3]Ac·CO △H<0
[Cu(NH3)3]Ac·CO △H<0
 NH3·H2O+H+达到平衡后,升高温度平衡正向移动
NH3·H2O+H+达到平衡后,升高温度平衡正向移动
 2NH3(g)ΔH<0达到平衡后,升高温度,反应速率v(H2)和H2的平衡转化率均增大
2NH3(g)ΔH<0达到平衡后,升高温度,反应速率v(H2)和H2的平衡转化率均增大
 CH(g)+H2(g) △H1="156.6" kJ/mol
CH(g)+H2(g) △H1="156.6" kJ/mol
 CH2(g)=CH4(g)+HC
CH2(g)=CH4(g)+HC
 CH(g ) △H2="32.4" kJ/mol
CH(g ) △H2="32.4" kJ/mol CH2(g)+H2(g)的△H= kJ/mol。
CH2(g)+H2(g)的△H= kJ/mol。 HCO3-+H+的平衡常数K1= 。(已知10-5.60=2.5×10-6)
HCO3-+H+的平衡常数K1= 。(已知10-5.60=2.5×10-6)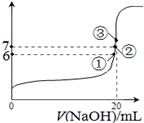
 SO2Cl2(l) △H=–97.3kJ·mol—1
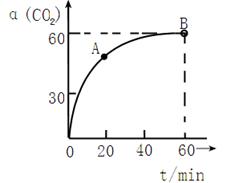
SO2Cl2(l) △H=–97.3kJ·mol—1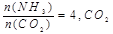 的转化率随时间的变化关系如图1所示。
的转化率随时间的变化关系如图1所示。 点速率为V正(CO2)(填“大于”、“小于”或“等于”)
点速率为V正(CO2)(填“大于”、“小于”或“等于”)