题目内容
【题目】下列离子方程式正确的是( )
A.向澄清石灰水中加入等物质的量的NaHCO3溶液:Ca2++2OH﹣+2HCO ![]() ═CaCO3↓+CO
═CaCO3↓+CO ![]() +2H2O
+2H2O
B.向NH4HSO4稀溶液中加入NaOH稀溶液少量:OH﹣+NH ![]() ═NH3?H2O
═NH3?H2O
C.氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+═Fe3++3H2O
D.向淀粉KI溶液中滴加酸性H2O2溶液,溶液变蓝色:H2O2+2I﹣+2H+═I2+2H2O
【答案】D
【解析】解:A.向澄清石灰水中加入等物质的量的NaHCO3溶液,离子方程式:Ca2++OH﹣+HCO ![]() ═CaCO3↓+H2O,故A错误; B.向NH4HSO4稀溶液中加入NaOH稀溶液少量,离子方程式:OH﹣+H+═H2O,故B错误;
═CaCO3↓+H2O,故A错误; B.向NH4HSO4稀溶液中加入NaOH稀溶液少量,离子方程式:OH﹣+H+═H2O,故B错误;
C.氢氧化铁溶于氢碘酸中的离子反应为:2I﹣+2Fe(OH)3+6H+═2Fe2++6H2O+I2 , 故C错误;
D.向淀粉KI溶液中滴加酸性H2O2溶液,溶液变蓝色,离子方程式:H2O2+2I﹣+2H+═I2+2H2O,故D正确;
故选:D.

 阅读快车系列答案
阅读快车系列答案【题目】合成氨技术的创立开辟了人工固氮的重要途径,其研究自正确的理论指导,合成氨反应N2+3H2![]() 2NH3的平衡常数K值和温度的关系如下:
2NH3的平衡常数K值和温度的关系如下:
温度/℃ | 360 | 440 | 520 |
K值 | 0.036 | 0.010 | 0.0038 |
(1)①由表中数据可知该反应为______反应(填“放热”或“吸热”)
②理论上,为了增大平衡时H2的转化率,可采取的措施是______________(填字母序号)。
a.增大压强 b.使用合适的催化剂
c.升高温度 d.及时分离出产物中的NH3
(2)原料气H2可通过反应CH4(g)+H2O(g) ![]() CO(g)+3H2(g)获取,已知该反应中,当初始混合气中的
CO(g)+3H2(g)获取,已知该反应中,当初始混合气中的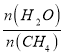 恒定时,温度、压强对平衡混合气中CH4含量的影响如图所示:
恒定时,温度、压强对平衡混合气中CH4含量的影响如图所示:

①图中,两条曲线表示压强的关系是p1________p2(填“>”、“=”或“<”)。
②该反应为________反应(填“吸热”或“放热”)。
(3)原料气H2还可通过反应CO(g)+H2O(g) ![]() CO2(g)+H2(g)获取。T ℃时,向容积固定为2 L的容器中充入1 mol水蒸气和1 mol CO,反应达平衡后,测得CO2的浓度为0.3 mol·L-1,则平衡时CO的转化率为________
CO2(g)+H2(g)获取。T ℃时,向容积固定为2 L的容器中充入1 mol水蒸气和1 mol CO,反应达平衡后,测得CO2的浓度为0.3 mol·L-1,则平衡时CO的转化率为________