题目内容
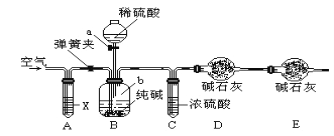
【题目】SO2通过下列工艺流程可制备化工原料H2SO4和清洁能源H2
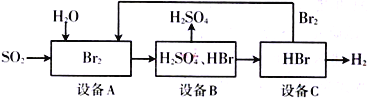
下列说法中不正确的是
A. 设备A中的溴水褪色,体现了SO2的还原性
B. 该生产工艺的优点:Br2可以循环利用,并获得清洁能源H2
C. 该工艺流程的总反应方程式为:SO2+Br2+2H2O=H2SO4+2HBr
D. 设备C中是否残余H2SO4,可在C的样品溶液中加入BaCl2溶液,观察是否有沉淀
【答案】C
【解析】A. 设备A中的溴水褪色,发生反应:SO2+Br2+2H2O=H2SO4+2HBr,体现了SO2的还原性,A正确;B. 根据转化关系图可判断该生产工艺的优点:Br2可以循环利用,并获得清洁能源H2,B正确;C. 由于溴单质可以循环利用,生成物实际上是硫酸和氢气,所以该工艺流程的总反应方程式为:SO2+2H2O=H2SO4+H2↑,C错误;D. 设备C中是否残余H2SO4,可在C的样品溶液中加入BaCl2溶液,观察是否有沉淀,D正确,答案选C。

练习册系列答案
相关题目