题目内容
【题目】设计如下实验探究某矿石(仅含四种短周期元素)的组成和性质,已知矿石含有一定的结晶水:
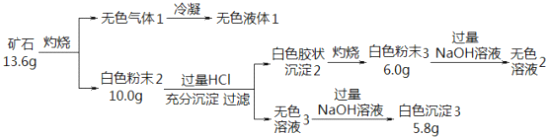
(1)矿石的组成元素是 H、O 和_____、 ______(填元素符号),化学式为_____________。
(2)白色粉末3 溶于NaOH溶液的离子方程式是_________。
【答案】 Mg Si MgSiO3·2H2O 2OH-+SiO2=SiO32-+H2O
【解析】根据流程图,矿石灼烧后生成无色气体1,冷凝后得到无色液体1,该无色液体为水,质量为3.6g,物质的量为0.2mol;白色粉末2能够溶于过量盐酸,得到白色胶状沉淀2,和无色溶液3;根据盐酸提供的氢离子和氯离子分析,白色胶状沉淀2可能是氯化银沉淀或硅酸沉淀;白色胶状沉淀2灼烧得到白色粉末3,该物质能够溶于氢氧化钠溶液,说明白色粉末为二氧化硅,不可能为氯化银,因此白色胶状沉淀2为硅酸;无色溶液3中加入过量氢氧化钠得到白色沉淀,说明白色沉淀3为氢氧化镁,5.8g氢氧化镁的物质的量为0.1mol,因此白色粉末2中含有4g氧化镁和6g二氧化硅,因此白色粉末2为硅酸镁。
(1)根据上述分析,矿石的组成元素是 H、O、Mg和Si,硅酸镁的质量为10g,物质的量为![]() =0.1mol,水的物质的量为
=0.1mol,水的物质的量为![]() =0.2mol,因此化学式为MgSiO3·2H2O,故答案为:Mg;Si;MgSiO3·2H2O;
=0.2mol,因此化学式为MgSiO3·2H2O,故答案为:Mg;Si;MgSiO3·2H2O;
(2)白色粉末3为二氧化硅, 溶于NaOH溶液的离子方程式为2OH-+SiO2=SiO32-+H2O,故答案为:2OH-+SiO2=SiO32-+H2O。

 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案【题目】POCl3是重要的基础化工原料,广泛用于制药、染料、表面活性剂等行业。一种制备POCl3的原理为:PCl3+Cl2+SO2=POCl3+SOCl2。某化学学习小组拟利用如下装置在实验室模拟制备POCl3。有关物质的部分性质如下:
物质 | 熔点/℃ | 沸点/℃ | 密度/g·mL-1 | 其它 |
PCl3 | -93.6 | 76.1 | 1.574 | 遇水强烈水解,易与氧气反应 |
POCl3 | 1.25 | 105.8 | 1.645 | 遇水强烈水解,能溶于PCl3 |
SOCl2 | -105 | 78.8 | 1.638 | 遇水强烈水解,加热易分解 |

(1)仪器甲的名称为______________,与自来水进水管连接的接口编号是________________。(填“a”或“b”)。
(2)装置C的作用是___________________,乙中试剂的名称为____________________。
(3)该装置有一处缺陷,解决的方法是在现有装置中再添加一个装置,该装置中应装入的试剂为_________(写名称)。若无该装置,则可能会有什么后果?请用化学方程式进行说明__________________________。
(4)D中反应温度控制在60-65℃,其原因是_______________。
(5)测定POCl3含量。①准确称取30.70gPOCl3产品,置于盛有60.00mL蒸馏水的水解瓶中摇动至完全水解;②将水解液配成100.00mL溶液,取10.00mL溶液于锥形瓶中;③加入10.00mL3.200mol/LAgNO3标准溶液,并加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖;④以Fe3+为指示剂,用0.2000mol/LKSCN溶液滴定过量的AgNO3溶液,达到滴定终点时共用去10.00mLKSCN溶液。
①滴定终点的现象为____________________,用硝基苯覆盖沉淀的目的是__________________。
②反应中POCl3的百分含量为__________________。
【题目】羰基硫(COS)常用作粮食熏蒸剂,制取反应为 CO(g)+H2S(g) ![]() COS(g)+H2(g),△H=-30kJ·mol-1。在恒容的密闭容器中不同条件下发生反应并达到平衡,数据如下表。
COS(g)+H2(g),△H=-30kJ·mol-1。在恒容的密闭容器中不同条件下发生反应并达到平衡,数据如下表。
实验 | 温度/℃ | n起始/mol | 平衡时 | 所需时间 | |||
CO | H2S | COS | H2 | n(CO)/mol | min | ||
1 | 150 | 10.0 | 10.0 | 0 | 0 | 7.0 | e |
2 | 150 | 7.0 | 7.0 | 3.0 | 3.0 | a | f |
3 | 200 | 20.0 | 20.0 | 0 | 0 | 16.0 | g |
下列说法错误的是
A. 实验1 反应开始到平衡整个过程中放出的热量为 90kJ
B. 实验2 达平衡时,a>7.0
C. 实验3 时间:g<e
D. 实验3 CO 达到平衡时的转化率比实验1 小