题目内容
下图为从反面看到的某套实验装置示意图,无法看到实验说明,加热装置已经省略。
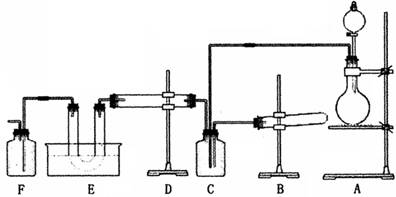
甲同认为此套装置用于合成物质X,E处冰水冷却的U型管中有固体X出现;乙同认为此套装置用于合成物质Y,E处冰水冷却的U型管中有红棕色气体Y生成,并且越接近U型管底部颜色越浅。对于A处,甲认为有加热装置,乙认为没有。
(1)事实上此装置所附实验说明符合甲同的推断,那么X的化式是 ,C装置中盛放的液体药品是 。
(2)甲同方案中为了提高A装置产物的转化率,可以增大B装置产物的通入量。要知道A、B两个装置产物的通入量哪个大,可通过观察 得知。
(3)若要用上述装置完成乙同所认为的实验,C处所起作用与合成X时所起作用一致,那么C处的广口瓶应改为 ,所装药品为 。
(4)写出乙同认为的D装置中发生反应的化方程式 。为什么此时U型管中的红棕色气体越接近管底颜色越浅?

甲同认为此套装置用于合成物质X,E处冰水冷却的U型管中有固体X出现;乙同认为此套装置用于合成物质Y,E处冰水冷却的U型管中有红棕色气体Y生成,并且越接近U型管底部颜色越浅。对于A处,甲认为有加热装置,乙认为没有。
(1)事实上此装置所附实验说明符合甲同的推断,那么X的化式是 ,C装置中盛放的液体药品是 。
(2)甲同方案中为了提高A装置产物的转化率,可以增大B装置产物的通入量。要知道A、B两个装置产物的通入量哪个大,可通过观察 得知。
(3)若要用上述装置完成乙同所认为的实验,C处所起作用与合成X时所起作用一致,那么C处的广口瓶应改为 ,所装药品为 。
(4)写出乙同认为的D装置中发生反应的化方程式 。为什么此时U型管中的红棕色气体越接近管底颜色越浅?
(1)SO3 浓硫酸
(2)C装置中哪个导管冒出气泡的速率快
(3)U型管(或干燥管) 碱石灰
(4)
 温度降低,2NO2
温度降低,2NO2 N2O4平衡向右移动。
N2O4平衡向右移动。 本题为开放型实验题。(1)E处冰水冷却的U型管中有固体X,则X为SO3,C装置的作用是干燥SO2和O2,所以为浓硫酸;(2)可以通过气体通入浓硫酸产生的气泡来衡量A、B两个装置产物的通入量的大小;(3)由乙同的叙述,气体Y是NO2,则从装置可知,进入C中的气体为NH3和O2,所以干燥剂为碱石灰,固体干燥剂用U型管来装;(4)D中发生的反应为氨气的催化氧化,生成的NO在U型管中继续与氧气反应,生成红棕色的NO2,由于存在平衡:2NO2
 N2O4,温度降低,平衡正向移动,颜色变浅。
N2O4,温度降低,平衡正向移动,颜色变浅。
练习册系列答案
相关题目