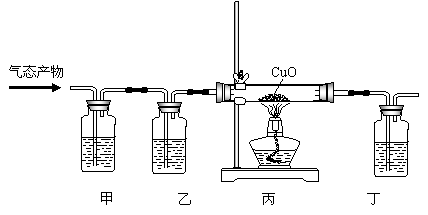
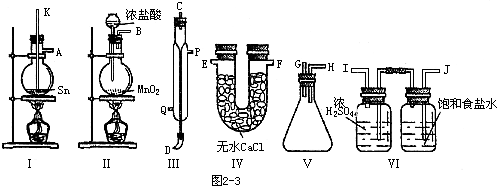
题目内容
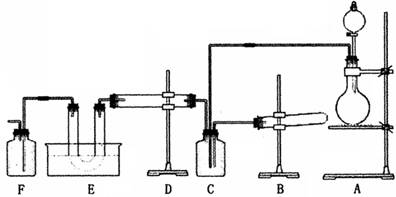
四氯化锡常温下是无色液体,在空气中极易水解,熔点-36℃,沸点114℃;金属锡的熔点为231℃,拟用以下仪器,设计组装一套实验装置,用熔融的金属锡跟干燥的氯气直接作用制取无水四氯化锡(此反应过程放出大量的热)请回答下列各个问题。
E.已知四氯化锡遇水强烈水解,产物之一是固态二氧化锡,那么四氯化锡水解的化学方程式为_______。
F.如果将制取的四氯化锡少许暴露于空气中,预期可看到的现象是________。
G.为了防止污染空气,在装置的最后应_______。

| A.用玻璃管(未画出)连接上述装置,正确的顺序是(填各接口的代字母) ( )接( )、( )接( )、( )接( )、( )接( )、( )接( ); |
| B.装置Ⅵ作用是______;装置Ⅳ的作用是______; |
| C.冷凝管里冷水的流向是从______进入,从________流出; |
| D.实验时应先点燃_______处酒精灯,加热温度应大于______℃,待_______即可停止加热; |
F.如果将制取的四氯化锡少许暴露于空气中,预期可看到的现象是________。
G.为了防止污染空气,在装置的最后应_______。
A.(B)接(J)、(I)接(K)、(A)接(C)、(D)接(G)、(H)接(E)或(F)
B.除去Cl2中的HCl和水气防止空气中水蒸气进入收集SnCl2的瓶内
C.Q.P
D.I,231,锡粒熔化
E.SnCl4+2H2O====SnO2+4HCl↑
F.有白色烟雾产生
G.用盛有NaOH溶液的烧杯吸收多余Cl2
B.除去Cl2中的HCl和水气防止空气中水蒸气进入收集SnCl2的瓶内
C.Q.P
D.I,231,锡粒熔化
E.SnCl4+2H2O====SnO2+4HCl↑
F.有白色烟雾产生
G.用盛有NaOH溶液的烧杯吸收多余Cl2
本题要完成的反应是:Sn(溶)+2Cl2(气)=SnCl4。
为此,应首先使(1)Sn熔化;(2)制备干燥纯净的Cl2气,并且根据题目的提示;要防止SnCl4水解和加热启动反应后由于放出热量大应停止继续加热。
审查题目所给的6个装置,依次为Ⅰ.反应装置;Ⅱ.造气装置;Ⅲ.冷凝装置,Ⅳ.干燥装置;Ⅴ.接受装置;Ⅵ.净化装置。
由此可以回答:A连接顺序:造气—净化—反应—冷凝—接收—干燥防潮,即Ⅱ—Ⅵ—Ⅰ—Ⅲ—Ⅴ—Ⅳ并找出正确接口,B,Ⅵ是净化Cl2的装置,当然应先经过饱和NaCl溶液,后经过浓H2SO4,如果接反了,将带出水气,使反应产率降低或失败,C,冷凝管斜置,夹套中的冷却水总是由下端Q进入,上端P流出,以提高冷却效率,D,启动反应应该先使金必属锡熔化,题目已给出了Sn的熔点,加热温度当然必须高于该温度,由于反应是在该蒸馏烧瓶中进行,而且跟Cl2反应,将会放出大量热量,所以当金属Sn熔化后,即应停止加热,E,四氯化锡的水解反应,应该是取代反应。
SnCl4+2H2O====SnO2+4HCl↑
F,SnCl4暴露在空气中,将吸收水气,生成SnO2白色微小固体,形成白烟,同时放出HCl气体,形成白雾,故有白色烟雾产生,G,反应中,难免有多余的Cl2逸出,因此,最后接上一个盛有碱液的吸收尾气的装置,反应为:
Cl2+2NaOH====NaClO+NaCl+H2O
为此,应首先使(1)Sn熔化;(2)制备干燥纯净的Cl2气,并且根据题目的提示;要防止SnCl4水解和加热启动反应后由于放出热量大应停止继续加热。
审查题目所给的6个装置,依次为Ⅰ.反应装置;Ⅱ.造气装置;Ⅲ.冷凝装置,Ⅳ.干燥装置;Ⅴ.接受装置;Ⅵ.净化装置。
由此可以回答:A连接顺序:造气—净化—反应—冷凝—接收—干燥防潮,即Ⅱ—Ⅵ—Ⅰ—Ⅲ—Ⅴ—Ⅳ并找出正确接口,B,Ⅵ是净化Cl2的装置,当然应先经过饱和NaCl溶液,后经过浓H2SO4,如果接反了,将带出水气,使反应产率降低或失败,C,冷凝管斜置,夹套中的冷却水总是由下端Q进入,上端P流出,以提高冷却效率,D,启动反应应该先使金必属锡熔化,题目已给出了Sn的熔点,加热温度当然必须高于该温度,由于反应是在该蒸馏烧瓶中进行,而且跟Cl2反应,将会放出大量热量,所以当金属Sn熔化后,即应停止加热,E,四氯化锡的水解反应,应该是取代反应。
SnCl4+2H2O====SnO2+4HCl↑
F,SnCl4暴露在空气中,将吸收水气,生成SnO2白色微小固体,形成白烟,同时放出HCl气体,形成白雾,故有白色烟雾产生,G,反应中,难免有多余的Cl2逸出,因此,最后接上一个盛有碱液的吸收尾气的装置,反应为:
Cl2+2NaOH====NaClO+NaCl+H2O

练习册系列答案
相关题目



 和CO;
和CO;