��Ŀ����
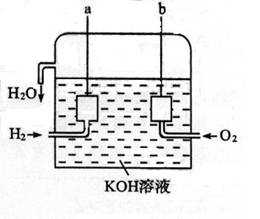
����ȼ�ϵ���ǽ�H2ͨ�븺����O2ͨ��������������ط�Ӧ�ģ�������ת���ʸߣ�
��1�����������ҺΪ���ᣬ��������ӦΪ_______������Ӧ������ת����2mol���ӣ��ɲ���ˮ������Ϊ______g��
��2����������ȼ�ϵ�ص����NaCl��CuSO4��ɵĻ����Һ��
����c��Na+��=3c��Cu2+��=0.3mol/L��ȡ�û��Һ100mL��ʯī���缫���е�⣬ͨ��һ��ʱ����������ռ���0.112L�������㵽��״�������壮��ʱ����ȼ�ϵ�����·��ת�Ƶ��ӵ����ʵ���Ϊ______mol���������ǵ�·�е�������ģ���
��1�����������ҺΪ���ᣬ��������ӦΪ_______������Ӧ������ת����2mol���ӣ��ɲ���ˮ������Ϊ______g��
��2����������ȼ�ϵ�ص����NaCl��CuSO4��ɵĻ����Һ��
����c��Na+��=3c��Cu2+��=0.3mol/L��ȡ�û��Һ100mL��ʯī���缫���е�⣬ͨ��һ��ʱ����������ռ���0.112L�������㵽��״�������壮��ʱ����ȼ�ϵ�����·��ת�Ƶ��ӵ����ʵ���Ϊ______mol���������ǵ�·�е�������ģ���
��1�����������Һ�����ᣬ�����������õ��Ӻ������ӷ�Ӧ����ˮ���缫��ӦʽΪ��O2+4H++4e-=2H2O������ת�Ƶ��Ӻ�ˮ֮��Ĺ�ϵʽ֪������ˮ������=
��2��18g/mol=18g��
�ʴ�Ϊ��O2+4H++4e-=2H2O��18��
��2���������ͭ���Ȼ��ƻ����Һʱ��������ͭ�����ȷŵ磬Ȼ�������ӷŵ�����������ͭ��ȫ����ʱת�Ƶ��ӵ����ʵ���=
��0.1L��2=0.02mol������0.112L����ת�Ƶ��ӵ����ʵ���=
��2=0.01mol��������·��ת�Ƶ�������ȣ���������ȼ�ϵ�����·��ת�Ƶ��ӵ����ʵ���Ϊ0.03mol��
�ʴ�Ϊ��0.03��
| 2mol |
| 4 |
�ʴ�Ϊ��O2+4H++4e-=2H2O��18��
��2���������ͭ���Ȼ��ƻ����Һʱ��������ͭ�����ȷŵ磬Ȼ�������ӷŵ�����������ͭ��ȫ����ʱת�Ƶ��ӵ����ʵ���=
| 0.3mol |
| 3 |
| 0.112L |
| 22.4Lmol |
�ʴ�Ϊ��0.03��

��ϰ��ϵ�д�
�����Ŀ

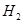 ��
��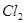 ��
��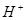 ��
�� ��
�� ��
��
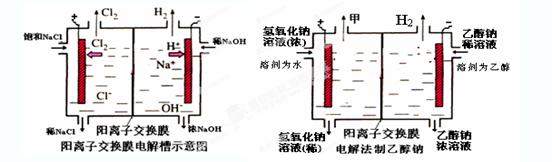
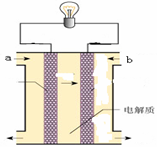
 2CO2+4H2O�����й��ڸõ�صķ������ټ״��Ǹ�����H+���ƶ��۸�����Ӧ��CH3OH-6e-+H2O=CO2+6H+ ��1 mol CH3OH��ȫ��Ӧת��12 mol���� ��������Ӧ��O2+4e-+2H2O==4OH-�õ�صĵ������Һ�����Ǽ�Һ��������ȷ����
2CO2+4H2O�����й��ڸõ�صķ������ټ״��Ǹ�����H+���ƶ��۸�����Ӧ��CH3OH-6e-+H2O=CO2+6H+ ��1 mol CH3OH��ȫ��Ӧת��12 mol���� ��������Ӧ��O2+4e-+2H2O==4OH-�õ�صĵ������Һ�����Ǽ�Һ��������ȷ���� Li2S2O4������˵����ȷ���ǣ� ��
Li2S2O4������˵����ȷ���ǣ� ��