��Ŀ����
�����ѣ�CH3OCH3������Ϊ21���͵���ࡢ��Ч��Դ��
�ϳɶ����ѷ�Ӧһ��3H2��g��+3CO��g��?CH3OCH3��g��+CO2��g����H=-247kJ/mol
һ�������¸÷�Ӧ���ܱ������дﵽƽ���Ҫ���CO��ת���ʣ����Բ�ȡ�Ĵ�ʩ��______��
A�����¸�ѹB���Ӵ���C������������N2 D������COŨ��E�������������
������ȼ�ϵ�صĹ���ԭ����ͼһ��ʾ��
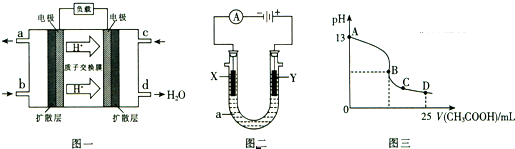
��1���õ�������ĵ缫��ӦʽΪ______������ڷŵ�����У�b��Ӧ�ĵ缫��Χ��Һ��pH______�������������С�����䡱��
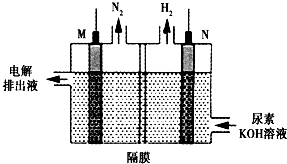
��2�����������Ϊ��Դ��ͨ��������ͼ������������
��X��YΪʯī��aΪ2L 0.1mol/LKCl��Һ��д������ܷ�Ӧ�����ӷ���ʽ��______��
��X��Y�ֱ�Ϊͭ������aΪ1L 0.2mol/LAgNO3��Һ��д��Y�缫��Ӧʽ��______��
��3������ʱ����������2���ٵ��һ��ʱ���ȡ25mL����������Һ���μ�0.2mol/L����õ�ͼ����������������ʧ����������ˮ����Һ����仯���Բ��ƣ���
�ٽ��ͼ�����㣬���������������Ķ����ѵ�����Ϊ______��
����ͼ����B��pH=7����ζ��յ���______���䣨�AB������BC����CD������
��C����Һ�и�����Ũ�ȴ�С��ϵ��______��
�ϳɶ����ѷ�Ӧһ��3H2��g��+3CO��g��?CH3OCH3��g��+CO2��g����H=-247kJ/mol
һ�������¸÷�Ӧ���ܱ������дﵽƽ���Ҫ���CO��ת���ʣ����Բ�ȡ�Ĵ�ʩ��______��
A�����¸�ѹB���Ӵ���C������������N2 D������COŨ��E�������������
������ȼ�ϵ�صĹ���ԭ����ͼһ��ʾ��

��1���õ�������ĵ缫��ӦʽΪ______������ڷŵ�����У�b��Ӧ�ĵ缫��Χ��Һ��pH______�������������С�����䡱��
��2�����������Ϊ��Դ��ͨ��������ͼ������������
��X��YΪʯī��aΪ2L 0.1mol/LKCl��Һ��д������ܷ�Ӧ�����ӷ���ʽ��______��
��X��Y�ֱ�Ϊͭ������aΪ1L 0.2mol/LAgNO3��Һ��д��Y�缫��Ӧʽ��______��
��3������ʱ����������2���ٵ��һ��ʱ���ȡ25mL����������Һ���μ�0.2mol/L����õ�ͼ����������������ʧ����������ˮ����Һ����仯���Բ��ƣ���
�ٽ��ͼ�����㣬���������������Ķ����ѵ�����Ϊ______��
����ͼ����B��pH=7����ζ��յ���______���䣨�AB������BC����CD������
��C����Һ�и�����Ũ�ȴ�С��ϵ��______��
I��Ҫ���CO��ת���ʣ��ı�����ʹ��Ӧ������Ӧ�����ƶ�������ͨ���ı��¶ȡ�ѹǿ��Ũ��ʹƽ��������Ӧ�����ƶ���
A�����¸�ѹƽ��������Ӧ�����ƶ������������CO��ת���ʣ�����ȷ��
B���Ӵ���ֻ�ܸı䷴Ӧ���ʣ����ܸı�ƽ���ƶ����ʴ���
C������������N2����Ӧ���������Ũ�Ȳ��䣬��ѧ��Ӧ���ƶ������Բ������CO��ת���ʣ��ʴ���
D������COŨ��ƽ��������Ӧ�����ƶ�����CO��ת���ʼ�С���ʴ���
E������������ѣ�������Ũ�ȼ�С��ƽ��������Ӧ�����ƶ����������CO��ת���ʣ�����ȷ��
��ѡAE��
II����1�������������ƶ�����֪����ߵ缫�Ǹ�����ͨ��ȼ�϶����ѣ��ұߵ缫��������ͨ����������������ȼ�ϵ���У������������õ��Ӻ������ӷ�Ӧ����ˮ���缫��ӦʽΪO2+4e-+4H+=2H2O��
����ڷŵ�����У�b��Ӧ�ĵ缫�϶�����ʧ�������������ӣ�����������Ũ����������Һ��pH��С��
�ʴ�Ϊ��O2+4e-+4H+=2H2O����С��
��2����X��YΪʯī���ŵ�ʱ�����������������ӷŵ硢�����������ӷŵ磬���Ե�ط�ӦʽΪ��2Cl-+2H2O
2OH-+H2��+Cl2�����ʴ�Ϊ��2Cl-+2H2O
2OH-+H2��+Cl2����
��X��Y�ֱ�Ϊͭ������Y����������������ʧ���ӷ���������Ӧ���缫��ӦʽΪAg-e-=Ag+��
�ʴ�Ϊ��Ag-e-=Ag+��
��3������ʱ����������2���ٵ��һ��ʱ���ȡ25mL����������Һ���μ�0.4mol/L����õ�ͼ����
�ٸ���ͼ֪��KOH��Һ��pH=13�������£�KOH��Ũ����0.1mol/L����n��KOH��=0.1mol/L��2L=0.2mol������2Cl-+2H2O
2OH-+H2��+Cl2��֪������0.2mol����������ת�Ƶ��ӵ����ʵ���=
��2=0.2mol��������ȼ�ϵ�ص��ܷ�Ӧ����ʽ��CH3OCH3+3O2=2CO2+3H2O��������ת��ΪCO2������1mol������ת�Ƶ�����=2��[4-��-2��]=12mol����˵�ת��0.2mol����ʱ���Ķ����ѵ�����=
��46g/mol=0.77g��
�ʴ�Ϊ��0.77g��
�ڵζ��յ����ǡ�÷�Ӧ����CH3COOK��KOH��Ũ���Ǵ����һ�룬��ǡ���к�ʱ��Ҫ����������KOH�����һ�룬�����Ϊǿ�������Σ�����Һ�ʼ��ԣ�����Һ��pH=7ʱ�����������������Դ����������KOH�����һ�룬���Եζ��յ�ΪAB�Σ��ʴ�Ϊ��AB��
��C����Һ��������c��H+����c��OH-������ϵ���غ�c��K+��+c��H+��=c��CH3COO-��+c��OH-�����õ�c��CH3COO-����c��K+����������Һ������Ũ�ȴ�С˳���ǣ�c��CH3COO-����c��K+����c��H+����c��OH-�����ʴ�Ϊ��c��CH3COO-����c��K+����c��H+����c��OH-����
A�����¸�ѹƽ��������Ӧ�����ƶ������������CO��ת���ʣ�����ȷ��
B���Ӵ���ֻ�ܸı䷴Ӧ���ʣ����ܸı�ƽ���ƶ����ʴ���
C������������N2����Ӧ���������Ũ�Ȳ��䣬��ѧ��Ӧ���ƶ������Բ������CO��ת���ʣ��ʴ���
D������COŨ��ƽ��������Ӧ�����ƶ�����CO��ת���ʼ�С���ʴ���
E������������ѣ�������Ũ�ȼ�С��ƽ��������Ӧ�����ƶ����������CO��ת���ʣ�����ȷ��
��ѡAE��
II����1�������������ƶ�����֪����ߵ缫�Ǹ�����ͨ��ȼ�϶����ѣ��ұߵ缫��������ͨ����������������ȼ�ϵ���У������������õ��Ӻ������ӷ�Ӧ����ˮ���缫��ӦʽΪO2+4e-+4H+=2H2O��
����ڷŵ�����У�b��Ӧ�ĵ缫�϶�����ʧ�������������ӣ�����������Ũ����������Һ��pH��С��
�ʴ�Ϊ��O2+4e-+4H+=2H2O����С��
��2����X��YΪʯī���ŵ�ʱ�����������������ӷŵ硢�����������ӷŵ磬���Ե�ط�ӦʽΪ��2Cl-+2H2O
| ||
| ||
��X��Y�ֱ�Ϊͭ������Y����������������ʧ���ӷ���������Ӧ���缫��ӦʽΪAg-e-=Ag+��
�ʴ�Ϊ��Ag-e-=Ag+��
��3������ʱ����������2���ٵ��һ��ʱ���ȡ25mL����������Һ���μ�0.4mol/L����õ�ͼ����
�ٸ���ͼ֪��KOH��Һ��pH=13�������£�KOH��Ũ����0.1mol/L����n��KOH��=0.1mol/L��2L=0.2mol������2Cl-+2H2O
| ||
| 0.2mol |
| 2 |
| 0.2mol |
| 12 |
�ʴ�Ϊ��0.77g��
�ڵζ��յ����ǡ�÷�Ӧ����CH3COOK��KOH��Ũ���Ǵ����һ�룬��ǡ���к�ʱ��Ҫ����������KOH�����һ�룬�����Ϊǿ�������Σ�����Һ�ʼ��ԣ�����Һ��pH=7ʱ�����������������Դ����������KOH�����һ�룬���Եζ��յ�ΪAB�Σ��ʴ�Ϊ��AB��
��C����Һ��������c��H+����c��OH-������ϵ���غ�c��K+��+c��H+��=c��CH3COO-��+c��OH-�����õ�c��CH3COO-����c��K+����������Һ������Ũ�ȴ�С˳���ǣ�c��CH3COO-����c��K+����c��H+����c��OH-�����ʴ�Ϊ��c��CH3COO-����c��K+����c��H+����c��OH-����

��ϰ��ϵ�д�
�����Ŀ